题目内容
3.下列表达方式正确的是( )| A. | CO2的分子模型示意图: | |
| B. | 硫原子的轨道表示式为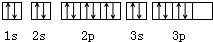 | |
| C. | 硫离子的核外电子排布式 1s22s22p63s23p4 | |
| D. | 碳-12原子构成 ${\;}_{6}^{12}$C |
分析 A.二氧化碳为直线形分子;
B.硫原子3p轨道电子排布违反洪特规则;
C.硫离子最外层8个电子;
D.碳-12原子,质子数6,质量数12.
解答 解:A.二氧化碳为直线形分子,三个原子在一条直线上,故A错误;
B.硫原子3p轨道电子排布违反洪特规则,后面两个电子应分占1个能级,故B错误;
C.硫离子的核外电子排布式 1s22s22p63s23p6,故C错误;
D.碳-12原子,质子数6,质量数12,原子构成 ${\;}_{6}^{12}$C,故D正确;
故选:D.
点评 本题考查分子空间构型、核外电子的排布,原子符号表示,侧重考查学生对常用化学用语熟练程度,明确各种符号表示方法是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
13.下列反应中,属于加成反应的是( )
| A. | 乙烷在光照下与氯气反应 | B. | 乙烯使酸性高锰酸钾溶液褪色 | ||
| C. | 乙烯使溴水褪色 | D. | 苯与液溴混合后撒入铁粉 |
14.下列物质属于纯净物的是( )
| A. | 铁锈 | B. | 氧化铁 | C. | 水银 | D. | 硬铝 |
11.下列说法错误的是( )
| A. | 重结晶时,溶液冷却速度越慢得到的晶体颗粒越大 | |
| B. | Cu2+与足量氨水反应的离子方程式 Cu2++2NH3•H2O═Cu(OH)2↓+2NH4+ | |
| C. | 抽滤装置由布氏漏斗、吸滤瓶、安全瓶、抽气泵等仪器组成,工作的主要原理是抽气泵给吸滤瓶减压,导致装置内部的压强降低,使过滤的速度加快 | |
| D. | 硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出 |
19.物质发生化学变化时:①电子总数②原子总数③分子总数④物质的种类⑤物质的总质量⑥物质的总能量,反应前后肯定不发生变化的是( )
| A. | ①②③⑤ | B. | ①②⑤ | C. | ②⑤⑥ | D. | ①④⑤⑥ |
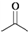 ,则
,则 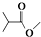 分子式:C5H8O2.
分子式:C5H8O2. .
. .
.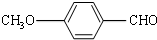 有多种同分异构体,其中属于芳香族羧酸的同分异构体共有4种,它们的结构简式是:
有多种同分异构体,其中属于芳香族羧酸的同分异构体共有4种,它们的结构简式是: 、
、 ;
; ,
, (任意两种)(任写其中二种).
(任意两种)(任写其中二种). .
.
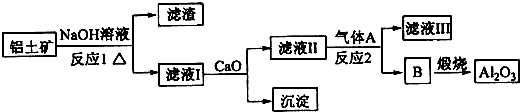
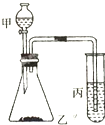 比较硫、碳、硅的非金属性由强到弱的顺序,请从下列给出的试剂中选择合理的实
比较硫、碳、硅的非金属性由强到弱的顺序,请从下列给出的试剂中选择合理的实