题目内容
8.在0.1mol•L-1CH3COOH溶液中存在如下电离平衡:CH3COOH?CH3COO-+H+,对于该平衡,下列叙述正确的是( )| A. | 加入少量NaOH固体,平衡向正反应方向移动 | |
| B. | 加入水,平衡向逆反应方向移动 | |
| C. | 加入少量0.1 mol•L-1HCl溶液,溶液中C(H+)减小 | |
| D. | 加入少量CH3COONa固体,平衡向正反应方向移动 |
分析 A.加入少量NaOH固体,与氢离子反应;
B.加水促进弱电解质的电离;
C.加盐酸抑制醋酸电离,但氢离子浓度增大;
D.加入少量CH3COONa固体,醋酸根离子浓度增大.
解答 解:A.加入少量NaOH固体,与氢离子反应,生成物浓度减小,则平衡向正反应方向移动,故A正确;
B.加水促进弱电解质的电离,则平衡正向移动,故B错误;
C.加入少量0.1 mol•L-1HCl溶液,平衡逆向移动,但c(H+)增大,故C错误;
D.加入少量CH3COONa固体,醋酸根离子浓度增大,则平衡逆向移动,故D错误;
故选A.
点评 本题考查化学平衡的影响因素,为高频考点,把握电离平衡移动、弱电解质电离为解答的关键,侧重分析与应用能力的考查,注意平衡移动原理的应用,题目难度不大.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
19.下列关于环境问题的说法不正确的是( )
| A. | 用甘蔗生产的乙醇燃料属于可再生能源,利用乙醇燃料不会产生温室气体 | |
| B. | 低碳生活注重节能减排,尽量使用太阳能等代替化石燃料,可减少雾霾的发生 | |
| C. | 太阳能、风能和生物能源属于新能源 | |
| D. | 太阳能电池可将太阳能直接转化为电能 |
19.根据如图的转化关系判断下列说法正确的是(反应条件已略去)( )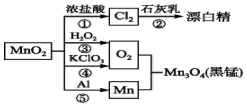

| A. | 反应①②③④⑤均属于氧化还原反应,反应③还属于置换反应 | |
| B. | 反应⑤说明该条件下铝可用于制熔点较高的金属 | |
| C. | 相同条件下生成等量的O2,反应③和④转移的电子数之比为1:1 | |
| D. | 反应①中氧化剂与还原剂的物质的量之比为1:4 |
3.下列有关电解质溶液的说法正确的是( )
| A. | 向盐酸中加入氨水至中性,溶液中$\frac{c(N{H}_{4}^{+})}{c(C{l}^{-})}$<1 | |
| B. | 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中$\frac{c(C{l}^{-})}{c(B{r}^{-})}$变大 | |
| C. | 将CH3COONa溶液加入水稀释后,溶液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)•c(O{H}^{-})}$不变 | |
| D. | 向0.1 mol•L-1 CH3COOH溶液从20℃升温至30℃,溶液中$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$减小 |
13.下列实验方案,不能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 检验食盐中是否添加KIO3 | 取食盐试样,溶于KI溶液,加入淀淀溶液,观察溶液是否变蓝 |
| B | 验证硝酸是挥发性酸 | 用两根玻璃棒分别蘸取浓硝酸和浓氨水,然后靠近,观察是否有白烟产生 |
| C | 验证Br2氧化性强于Fe3+ | 取少许FeCl2晶体溶于稀盐酸,加入KSCN观察溶液是否变红,滴入溴水后再观察是否变红 |
| D | 检验氯酸钾中含有氯元素 | 取少量氯酸钾加入MnO2充分加热,残留物溶于水,取上层清液,滴入硝酸酸化的AgNO3溶液,观察是否有白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
17.下列图示与对应的叙述相符的是( )
| A. | 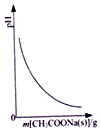 图表示向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化 | |
| B. | 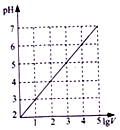 图表示0.1LpH=2的HC1溶液加水稀释至VL,pH随lgV的变化 | |
| C. | 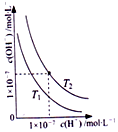 图表示不同温度下水溶液中H+和OH-浓度变化的曲线,图中温度T2>T1 | |
| D. | 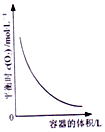 图表示同一温度下,再不同容积的容器中进行反应2BaO2(s)?2BaO(S)+O2(g),O2的平衡浓度与容器容积的关系 |
18.下列过程中反应离子方程式正确的是( )
| A. | 用漂白液漂洗衣物:H2O+2NaClO+CO2═2HClO+CO32-+2Na+ | |
| B. | 用碳酸钠溶液浸泡锅炉水垢:CaSO4(S)+CO32-(aq)?CaCO3(S)+SO42-(aq) | |
| C. | 用氢氧化钠溶液处理工业含二氧化硫的尾气:SO2+2OH-═HSO3-+H2O | |
| D. | 用加少量铁粉的方法存放硫酸亚铁溶液:Fe3++Fe═2Fe2+ |
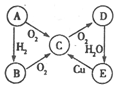 A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.
A、B、C、D、E五种物质中含有同一种元素,其相互转化关系如图所示.