题目内容
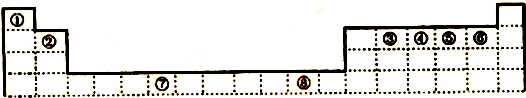
下表列出了①-⑨九种元素在周期表中的位置.

(1)⑨的原子结构示意图是 ;
(2)②、③、⑤的原子半径由大到小的顺序是 (填元素符合);
(3)④、⑦、⑧的气态氢化物的稳定性由强到弱的顺序是 (填化学式);
(4)④和⑥形成化合物的电子式是 ;
(5)⑤和⑥中金属性较弱的是 (填化学式);为了证明此结论,可以分别将⑤和⑥的单质加入 (填最佳试剂的化学式)中;
(6)A是只由①、②两元素组成的中学化学常见化合物,其中两种元素的原子个数比为1:1,A的摩尔质量在60g/mol-80g/mol之间,且不能使高锰酸钾溶液褪色,则A的分子式是 ;A能与③的最高价氧化物对应的水化物在一定条件下发生反应,其化学方程式为(注明具体的反应条件) .

(1)⑨的原子结构示意图是
(2)②、③、⑤的原子半径由大到小的顺序是
(3)④、⑦、⑧的气态氢化物的稳定性由强到弱的顺序是
(4)④和⑥形成化合物的电子式是
(5)⑤和⑥中金属性较弱的是
(6)A是只由①、②两元素组成的中学化学常见化合物,其中两种元素的原子个数比为1:1,A的摩尔质量在60g/mol-80g/mol之间,且不能使高锰酸钾溶液褪色,则A的分子式是
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中位置知①为H、②为C、③为N、④为F、⑤为Na、⑥为Mg、⑦为S、⑧为Cl、⑨为Ar.
(1)⑨为Ar,原子核外有3个电子层,各层电子数为2、8、8;
(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大;
(3)非金属性越强,氢化物越稳定;
(4)④和⑥形成化合物为MgF2,由镁离子与氟离子构成;
(5)同周期自左而右金属性减弱,可以根据金属单质与水反应剧烈程度证明;
(6)A是只由①、②两元素组成的中学化学常见化合物,其中两种元素的原子个数比为1:1,A的摩尔质量在60g/mol-80g/mol之间,且不能使高锰酸钾溶液褪色,则A为C6H6;C6H6与浓硝酸在浓硫酸、加热条件下生成硝基苯与水.
(1)⑨为Ar,原子核外有3个电子层,各层电子数为2、8、8;
(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大;
(3)非金属性越强,氢化物越稳定;
(4)④和⑥形成化合物为MgF2,由镁离子与氟离子构成;
(5)同周期自左而右金属性减弱,可以根据金属单质与水反应剧烈程度证明;
(6)A是只由①、②两元素组成的中学化学常见化合物,其中两种元素的原子个数比为1:1,A的摩尔质量在60g/mol-80g/mol之间,且不能使高锰酸钾溶液褪色,则A为C6H6;C6H6与浓硝酸在浓硫酸、加热条件下生成硝基苯与水.
解答:
解:由元素在周期表中位置知①为H、②为C、③为N、④为F、⑤为Na、⑥为Mg、⑦为S、⑧为Cl、⑨为Ar.
(1)⑨为Ar,原子核外有3个电子层,各层电子数为2、8、8,原子结构示意图为: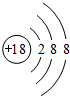 ,故答案为:
,故答案为: ;
;
(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:Na>C>N,故答案为:Na>C>N;
(3)同周期自左而右非金属性增强,同主族自上而下非金属性减弱,非金属性越强,氢化物越稳定,故氢化物稳定性:HF>HCl>H2S,故答案为:HF>HCl>H2S;
(4)④和⑥形成化合物为MgF2,由镁离子与氟离子构成,电子式为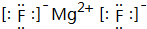 ,故答案为:
,故答案为: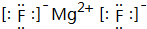 ;
;
(5)同周期自左而右金属性减弱,故金属性Na>Mg,可以根据金属单质与水反应剧烈程度证明,故答案为:Mg;H2O;
(6)A是只由①、②两元素组成的中学化学常见化合物,其中两种元素的原子个数比为1:1,A的摩尔质量在60g/mol-80g/mol之间,且不能使高锰酸钾溶液褪色,则A为C6H6;C6H6与浓硝酸在浓硫酸、加热条件下生成硝基苯与水,反应方程式为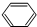 +HNO3
+HNO3
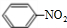 +H2O,
+H2O,
故答案为:C6H6; +HNO3
+HNO3
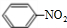 +H2O.
+H2O.
(1)⑨为Ar,原子核外有3个电子层,各层电子数为2、8、8,原子结构示意图为:
 ,故答案为:
,故答案为: ;
;(2)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径:Na>C>N,故答案为:Na>C>N;
(3)同周期自左而右非金属性增强,同主族自上而下非金属性减弱,非金属性越强,氢化物越稳定,故氢化物稳定性:HF>HCl>H2S,故答案为:HF>HCl>H2S;
(4)④和⑥形成化合物为MgF2,由镁离子与氟离子构成,电子式为
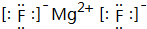 ,故答案为:
,故答案为: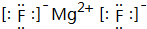 ;
;(5)同周期自左而右金属性减弱,故金属性Na>Mg,可以根据金属单质与水反应剧烈程度证明,故答案为:Mg;H2O;
(6)A是只由①、②两元素组成的中学化学常见化合物,其中两种元素的原子个数比为1:1,A的摩尔质量在60g/mol-80g/mol之间,且不能使高锰酸钾溶液褪色,则A为C6H6;C6H6与浓硝酸在浓硫酸、加热条件下生成硝基苯与水,反应方程式为
 +HNO3
+HNO3| 浓硫酸 |
| △ |
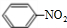 +H2O,
+H2O,故答案为:C6H6;
 +HNO3
+HNO3| 浓硫酸 |
| △ |
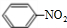 +H2O.
+H2O.
点评:本题考查元素周期表与元素周期律应用,难度不大,侧重对元素周期律的考查,注意掌握金属性、非金属性强弱比较及实验事实.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A、S(s)+O2(g)=SO2 (g);△H1 S(g)+O2(g)=SO2 (g);△H2 | ||||
| B、2H2(g)+O2 (g)=2H2O(g);△H1 2H2 (g)+O2 (g)=2H2O(l);△H2 | ||||
| C、CO(g)+1/2 O2(g)=CO2(g);△H1 2CO(g)+O2(g)=2CO2(g);△H2 | ||||
D、H2 (g)+Cl2(g)=2HCl(g);△H1
|
将BaO2放入密闭真空容器中,反应2BaO2(s)?2BaO(s)+O2(g)达到平衡,保持温度不变,缩小容器容积,体系重新达到平衡,下列说法正确的是( )
| A、平衡常数减小 |
| B、BaO量不变 |
| C、氧气压强减小 |
| D、BaO2量增加 |
绚丽的焰火将上海世博会开幕式推向了高潮.焰火与高中化学中“焰色反应”知识有关.下列有关“焰色反应”说法中正确的是( )
| A、焰色反应为化学变化 |
| B、所有金属及其化合物灼烧时火焰均有颜色 |
| C、NaCl与Na2CO3灼烧时火焰颜色相同 |
| D、焰色反应均应透过蓝色钴玻璃观察 |