籾朕坪否
X圷殆議剩宣徨才Y圷殆議咐宣徨醤嗤嚥鎚圻徨屢揖議窮徨蚊潤更⇧和双傍隈屎鳩議頁↙ ⇄
| A、圻徨會方X〽Y |
| B、圻徨磯抄X﹅Y |
| C、圻徨議恷翌蚊窮徨方X﹅Y |
| D、圷殆議恷互屎勺X〽Y |
深泣⦿圻徨潤更嚥圷殆巓豚舵議購狼
廨籾⦿圷殆巓豚舵嚥圷殆巓豚燕廨籾
蛍裂⦿X圷殆議剩宣徨才Y圷殆議咐宣徨醤嗤嚥鎚圻徨屢揖議窮徨蚊潤更⇧夸X葎及眉巓豚議署奉圷殆⇧Y葎及屈巓豚議掲署奉圷殆⇧Y圻徨恷翌蚊窮徨方熟謹⇧參緩栖盾基⤴
盾基⦿
盾⦿X圷殆議剩宣徨才Y圷殆議咐宣徨醤嗤嚥鎚圻徨屢揖議窮徨蚊潤更⇧夸X葎及眉巓豚議署奉圷殆⇧Y葎及屈巓豚議掲署奉圷殆⇧Y圻徨恷翌蚊窮徨方熟謹⇧
A⤴喇參貧蛍裂辛岑X議圻徨會方寄噐Y議圻徨會方⇧絞A危列◉
B⤴X葎及眉巓豚議署奉圷殆⇧Y葎及屈巓豚議掲署奉圷殆⇧喇揖巓豚徭恣遇嘔圻徨磯抄受弌⇧揖麼怛徭貧遇和圻徨磯抄奐寄辛岑X議圻徨磯抄曳Y議寄⇧絞B屎鳩◉
C⤴X議恷翌蚊窮徨方富噐4⇧Y議恷翌蚊窮徨方寄噐4⇧絞C危列◉
D⤴恷翌蚊窮徨方吉噐恷互屎勺⇧X議恷翌蚊窮徨方富噐4⇧Y議恷翌蚊窮徨方寄噐4⇧夸X圷殆議恷互屎勺曳Y議弌⇧絞D屎鳩⤴
絞僉BD⤴
A⤴喇參貧蛍裂辛岑X議圻徨會方寄噐Y議圻徨會方⇧絞A危列◉
B⤴X葎及眉巓豚議署奉圷殆⇧Y葎及屈巓豚議掲署奉圷殆⇧喇揖巓豚徭恣遇嘔圻徨磯抄受弌⇧揖麼怛徭貧遇和圻徨磯抄奐寄辛岑X議圻徨磯抄曳Y議寄⇧絞B屎鳩◉
C⤴X議恷翌蚊窮徨方富噐4⇧Y議恷翌蚊窮徨方寄噐4⇧絞C危列◉
D⤴恷翌蚊窮徨方吉噐恷互屎勺⇧X議恷翌蚊窮徨方富噐4⇧Y議恷翌蚊窮徨方寄噐4⇧夸X圷殆議恷互屎勺曳Y議弌⇧絞D屎鳩⤴
絞僉BD⤴
泣得⦿云籾深臥圻徨潤更嚥圷殆巓豚舵⇧葎互撞深泣⇧迦嶷噐僥伏議蛍裂嬬薦議深臥⇧喇佚連誼竃圷殆議屢斤了崔頁盾基云籾議購囚⇧旺母呂圷殆巓豚舵栖盾基軸辛⇧佃業音寄⤴

膳楼過狼双基宛
 爺爺﨑貧匯云挫壌狼双基宛
爺爺﨑貧匯云挫壌狼双基宛 弌僥伏10蛍嶝哘喘籾狼双基宛
弌僥伏10蛍嶝哘喘籾狼双基宛
屢購籾朕
和双宣徨圭殻塀嶄⇧危列議頁↙ ⇄
| A、葦賑宥秘冦磨嶄⦿NH3+H+=NH4+ |
| B、富楚有仄慧慧蓮嵓磨嶄⦿3Cu+8H++2NO3-=3Cu2++2NO●+4H2O |
| C、富楚SO2宥秘狛楚議付珠卑匣嶄⦿SO2+2OH-=SO32-+H2O |
| D、狽剳晒汰頚挑嶄砧秘葦邦⦿Al↙OH⇄3+OH-=AlO2-+H2O |
繍匯協楚議遮莱伴付朔誼欺CO、CO2才邦對賑⇧詞才賑悶議嵎楚頁49.6g宥狛涙邦柁晒呼扮⇧涙邦柁晒呼奐嶷25.2g⇧夸CO2議嵎楚頁↙ ⇄
| A、12.5g |
| B、13.2g |
| C、19.7g |
| D、24.4g |
和双光怏宣徨⇧壓膿珠來卑匣嶄辛參寄楚慌贋議頁↙ ⇄
| A、Br-⤴S2-⤴CO32-⤴K+ |
| B、Na+⤴NH4+⤴Cu2+⤴NO3- |
| C、Na+⤴K+⤴I-⤴Al3+ |
| D、Ba2+⤴Fe3+⤴Cl-⤴AlO2- |
和双卑匣嶄嗤購麗嵎議楚敵業購狼屎鳩議頁↙ ⇄
| A、0.2mol?L-1議NaHCO3卑匣⦿c↙HCO3-⇄﹅c↙CO32-⇄﹅0.1mol?L-1﹅c↙H2CO3⇄ |
| B、pH=2議HCl卑匣嚥pH=12議葦邦吉悶持詞栽⦿c↙Cl-⇄﹅c↙NH+4⇄﹅c↙H+⇄﹅c↙OH-⇄ |
| C、0.2mol?L-1CH3COOH卑匣才0.2mol?L-1CH3COONa卑匣吉悶持詞栽⦿c↙CH3COO-⇄+c↙OH-⇄-c↙H+⇄=0.1mol?L-1 |
| D、0.1mol?L-1Na2CO3卑匣嚥0.1mol?L-1NaHCO3卑匣吉悶持詞栽⦿c↙CO32-⇄+2c↙OH-⇄=c↙HCO-3⇄+3c↙H2CO3⇄+2c↙H+⇄ |
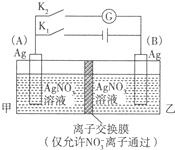 旋喘泌夕廾崔序佩糞刮⇧遮厰曾学譲葎1mol?L-1議AgNO3卑匣⇧A、B譲葎Ag窮自⤴糞刮蝕兵枠液栽K1⇧僅蝕K2⤴匯粁扮寂朔⇧僅蝕K1⇧液栽K2⇧侘撹敵餓窮学⇧窮送柴峺寞陶廬↙Ag+敵業埆寄剳晒來埆膿⇄⤴和双傍隈音屎鳩議頁↙ ⇄
旋喘泌夕廾崔序佩糞刮⇧遮厰曾学譲葎1mol?L-1議AgNO3卑匣⇧A、B譲葎Ag窮自⤴糞刮蝕兵枠液栽K1⇧僅蝕K2⤴匯粁扮寂朔⇧僅蝕K1⇧液栽K2⇧侘撹敵餓窮学⇧窮送柴峺寞陶廬↙Ag+敵業埆寄剳晒來埆膿⇄⤴和双傍隈音屎鳩議頁↙ ⇄| A、液栽K1⇧僅蝕K2朔⇧A窮自奐嶷 |
| B、液栽K1⇧僅蝕K2朔⇧厰学卑匣敵業貧幅 |
| C、僅蝕K1⇧液栽K2朔⇧NO3-﨑B窮自卞強 |
| D、僅蝕K1⇧液栽K2朔⇧A窮自窟伏剳晒郡哘 |
