题目内容
由0.1mol两种气态烃组成的混合气体,完全燃烧得0.16molCO2和3.6gH2O,下列说法正确的是( )
| A、混合气体中一定含有甲烷 |
| B、混合气体中一定是甲烷和乙烯 |
| C、混合气体中一定有乙烷 |
| D、混合气体中一定有乙炔 |
考点:有关混合物反应的计算
专题:烃及其衍生物的燃烧规律
分析:3.6g水的物质的量为:
=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,根据元素守恒,则混合烃的平均分子式为C1.6H4,而碳原子数小于1.6的只有甲烷,判断混合气体中一定含有甲烷,根据氢原子平均数目可知另一种烃分子中一定含有4个H原子,结合选项判断.
| 3.6g |
| 18g/mol |
解答:
解:3.6g水的物质的量为:
=0.2mol,即0.1mol混合烃完全燃烧生成0.16molCO2和0.2molH2O,根据元素守恒,则混合烃的平均分子式为C1.6H4,而碳原子数小于1.6的只有甲烷,判断混合气体中一定含有甲烷,根据氢原子平均数目可知另一种烃分子中一定含有4个H原子,可能为乙烯、丙炔等,一定不可能为乙烷,故A正确,BCD错误,故选A.
| 3.6g |
| 18g/mol |
点评:本题考查有机物分子式的确定,涉及混合烃组成的判断,难度中等,注意根据平均分子式进行判断,侧重考查学生分析解决问题的能力.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
在一定温度下,将气体X和气体Y 各0.16mol充入10L 恒容密闭容器中,发生反应X(g)+Y(g)?2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如下表下列说法正确的是( )
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A、反应前2min的平均速率v(Z)=0.04 mol/(L?min) |
| B、其他条件不变,升高温度,v(逆)增大,v(正)减小 |
| C、该温度下此反应的平衡常数K=1.44 |
| D、其他条件不变,再充入0.2 mol Z,平衡时X的体积分数增大 |
针对如图所示乙醇分子结构,下述关于乙醇在各种化学反应中化学键断裂情况的说法不正确的是( )
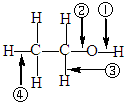

| A、与醋酸、浓硫酸共热时,②键断裂 |
| B、与金属钠反应时,①键断裂 |
| C、与浓硫酸共热至170℃时,②、④键断裂 |
| D、在Ag催化下与O2反应时,①、③键断裂 |
常温下,纯水中存在电离平衡:H2O?H++OH-.欲使水的电离平衡向正方向移动,并使c(H+)增大,应加入的物质是( )
| A、FeCl3 |
| B、H2SO4 |
| C、NaHCO3 |
| D、NaOH |
下列有关实验室一般事故的预防和处理方法正确的是( )
| A、燃着的酒精灯打翻失火,应立即用水浇灭 |
| B、为了使过滤速率加快,可用玻棒在过滤器中轻轻搅拌,加速液体流动 |
| C、蒸发食盐溶液时,发生液滴飞溅现象,应立即加水冷却 |
| D、皮肤上沾有少量浓硫酸,可立即用大量水冲洗 |
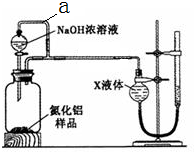 氮化铝(AlN)是一种新型无机材料.
氮化铝(AlN)是一种新型无机材料.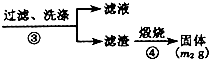
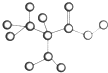 如图是某种只含有C、H、O、N的有机物简易球棍模型.请回答下列各题.
如图是某种只含有C、H、O、N的有机物简易球棍模型.请回答下列各题.