题目内容
14.${\;}_{\;}^{16}$O和${\;}_{\;}^{18}$O是氧元素的两种核素,下列说法正确的是( )| A. | ${\;}_{\;}^{16}$O与${\;}_{\;}^{18}$O与互为同位素 | |
| B. | ${\;}_{\;}^{16}$O与${\;}_{\;}^{18}$O核外电子排布方式不同 | |
| C. | 通过化学变化可以实现${\;}_{\;}^{16}$O与${\;}_{\;}^{18}$O间的相互转化 | |
| D. | 标准状况下,1.12L${\;}_{\;}^{16}$O2和1.12L${\;}_{\;}^{18}$O2含有相同的氧原子个数 |
分析 A、同种元素的不同种原子互称同位素;
B、16O与18O互为同位素,核外具有相同的电子数;
C、化学变化的最小微粒是原子;
D、标准状况下,气体的摩尔体积相同.
解答 解:A、${\;}_{\;}^{16}$O与${\;}_{\;}^{18}$O是同种元素的不同种原子,互称同位素,故A正确;
B、16O与18O互为同位素,核外具有相同的电子数,故核外电子排布相同,故B错误;
C、化学变化的最小微粒是原子,故实现16O与18O间的相互转化无法通过化学变化来实现,故C错误;
D、标准状况下,气体的摩尔体积相同,气体体积相同,则气体的物质的量相同,16O2和18O2均为双原子分子,所以含有相同的氧原子个数,故D正确;
故选AD.
点评 本题考查原子结构和核素、熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
2.重水(D20)是重要的核工业原料,下列说法错误的是( )
| A. | 氘(D)原子核外有1个电子 | |
| B. | H与D互称同位素 | |
| C. | H2O与D2O互称同素异形体 | |
| D. | 1H218O与D216O的相对分子质量相同 |
19.某合作学习小组讨论辨析以下说法:①粗盐和酸雨都是混合物;②天然气是可再生能源;③冰和干冰既是纯净物又是化合物;④不锈钢和目前流通的硬币都是合金;⑤盐酸和食醋既是化合物又是酸;⑥纯碱和熟石灰都是碱;⑦豆浆和雾都是胶体.上述说法正确的是( )
| A. | ①②③④ | B. | ①②⑤⑥ | C. | ③⑤⑥⑦ | D. | ①③④⑦ |
6.现有部分短周期元素的性质或原子结构如下表
(1)元素T的阴离子的结构示意图 .
.
(2)元素Y在周期表中的位置是第二周期ⅤA族.
(3)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示).下列表述中能证明这一事实的是bce.
a.常温下Z的单质和T的单质状态不同 b.Z的氢化物比T的氢化物稳定
c.Z的最高价氧物所对应的水化物比T的最高价氧化物所对应的水化物的酸性强
d.Z的氢化物笔比T的氢化物溶解度大
e.Z的单质与H2化合比T的单质与H2化合更容易
(4)结合所学的知识,请设计一个与(3)中的事实不同的实验方案证明元素Z与元素T的非金属性的强弱将氯气通入到Na2S溶液中,若产生淡黄色沉淀,则证明非金属性Cl>S.
| 元素编号 | 元素性质或原子结构 |
| T | M层的电子数为K层电子数的3倍 |
| X | 其化合物的种类最多且其氢化物是一种清洁能源 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价+7价 |
 .
.(2)元素Y在周期表中的位置是第二周期ⅤA族.
(3)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示).下列表述中能证明这一事实的是bce.
a.常温下Z的单质和T的单质状态不同 b.Z的氢化物比T的氢化物稳定
c.Z的最高价氧物所对应的水化物比T的最高价氧化物所对应的水化物的酸性强
d.Z的氢化物笔比T的氢化物溶解度大
e.Z的单质与H2化合比T的单质与H2化合更容易
(4)结合所学的知识,请设计一个与(3)中的事实不同的实验方案证明元素Z与元素T的非金属性的强弱将氯气通入到Na2S溶液中,若产生淡黄色沉淀,则证明非金属性Cl>S.
3.下列物质的结构或性质描述正确的是( )
| A. | 甲烷和氯气可以发生取代反应 | B. | 乙烯和高锰酸钾可以发生加成反应 | ||
| C. | 酯化反应中醇脱羟基酸脱氢 | D. | 乙醇可以发生银镜反应 |
4.X、Y、Z、M、N是元素周期表中的短周期主族元素,且原子序数依次递增.已知X的最外层电子数是次外层电子数的3倍,X、M同主族,Y在同周期主族元素中原子半径最大,Z和N可以形成ZN2型化合物.下列有关说法正确的是( )
| A. | X与Y只能形成一种化合物 | |
| B. | 最高价氧化物对应水化物的碱性:Y>Z | |
| C. | 单质熔点:M<N | |
| D. | 单质的氧化性:X<M |
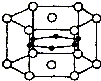 图为硼和镁两种元素组成的超导材料的晶体结构单元示意图,其中该化合物镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子,6个硼原子位于棱柱内.则该化合物的化学式可表示为MgB2.
图为硼和镁两种元素组成的超导材料的晶体结构单元示意图,其中该化合物镁原子间形成正六棱柱,且棱柱的上下底面还各有1个镁原子,6个硼原子位于棱柱内.则该化合物的化学式可表示为MgB2.