题目内容
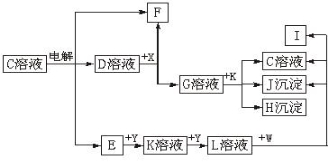
(10分)图中C至L分别表示反应中的一种常见物质,E、F、I在通常情况下是气体单质,其中E有刺激性气味,X、Y是常见的金属单质。W是由甲、乙元素按1∶1的比例组成的,其中甲元素的原子的M层电子数是K层的一半,乙元素的原子最外层电子数是次外层电子数的3倍。(参加反应的水和生成的水已从图中略去)
填写空白:
(1)E是___________(化学式),Y元素在周期表中的位置是______________________。
(2写出K+G H+J+C的离子方程式___________________________________________ 。
H+J+C的离子方程式___________________________________________ 。
(3)写出W+L J+C+I的化学方程式___________________________________________。
J+C+I的化学方程式___________________________________________。
(4)设计实验分离H和J(写出所用试剂和操作方法):______________________________。
(1)Cl2 (2分) 第四周期第Ⅷ族 (2分)
(2)3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓(2分)
(3)4Na2O2+4FeCl2+6H2O=4Fe(OH)3↓+8NaCl+O2↑(2分)
(4)NaOH、CO2;①向混合物中加足量的NaOH溶液过滤洗涤滤渣得Fe(OH)3
②向滤液中通入足量的CO2过滤洗涤滤渣得Al(OH)3(2分
【解析】
试题分析:根据框图中各种物质的转化关系及题意可知:X是Al;Y是Fe;W是Na2O2;C是NaCl;D是NaOH;E是Cl2;F是H2;G是NaAlO2;K是FeCl3;L是FeCl2;J是Fe(OH)3;I是O2;H 是Al(OH)3。(1)E是Cl2,Fe元素在周期表中的位置是第四周期第Ⅷ族; (2 K+G H+J+C的离子方程式是3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓;(3)W+L
H+J+C的离子方程式是3AlO2-+Fe3++6H2O=3Al(OH)3↓+Fe(OH)3↓;(3)W+L J+C+I的化学方程式是4Na2O2+4FeCl2+6H2O=4Fe(OH)3↓+8NaCl+O2↑;(4)Al(OH)3能够与强碱发生反应产生可溶性物质,而Fe(OH)3不能与强碱发生反应,所以分离H和J所用试剂是NaOH、CO2,操作方法是向混合物中加足量的NaOH溶液,过滤、洗涤滤渣得Fe(OH)3;②向滤液中通入足量的CO2过滤洗涤滤渣得Al(OH)3。
J+C+I的化学方程式是4Na2O2+4FeCl2+6H2O=4Fe(OH)3↓+8NaCl+O2↑;(4)Al(OH)3能够与强碱发生反应产生可溶性物质,而Fe(OH)3不能与强碱发生反应,所以分离H和J所用试剂是NaOH、CO2,操作方法是向混合物中加足量的NaOH溶液,过滤、洗涤滤渣得Fe(OH)3;②向滤液中通入足量的CO2过滤洗涤滤渣得Al(OH)3。
考点:考查物质的相互转化、推断、元素在周期表中的位置、化学方程式和离子方程式的书写、混合物分离方法及试剂的的选择的知识。

 xC(g)
xC(g)