题目内容
等物质的量的钠、镁、铝分别与1L1mol/L的盐酸作用产生氢气,可出现下列四种情况:①Na<Mg<Al;②Na<Mg=Al;③Na=Mg=Al;④Na>Mg=Al.讨讨论上述四种情况所需金属的物质的量分别在何范围?
①n<1/2 ② 1/2≤n<1
![]() ③n=1 ④n>1
③n=1 ④n>1
解析:
化学反应中,反应物与生成物的量通常成线性关系,作图时可利用特殊点(如刚开始反应,恰好完全反应等)画出投入金属量与产生氢气量的关系图,各种情况一目了然.
![]()
![]() 根据Na~H+~ H2 Mg~2H+~H2
根据Na~H+~ H2 Mg~2H+~H2
![]() Al~3H+~ H2
Al~3H+~ H2
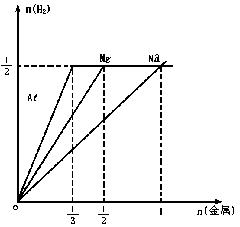
![]() 对于Na:起点O(0,0),盐酸恰好完全反应时为A点(1,1/2 );
对于Na:起点O(0,0),盐酸恰好完全反应时为A点(1,1/2 );
![]() 对于Mg:起点O(0,0),盐酸恰好完全反应时为B点( 1/2、1/2 );
对于Mg:起点O(0,0),盐酸恰好完全反应时为B点( 1/2、1/2 );
![]() 对于Al:起点O(0,0),盐酸恰好完全反应时为C点(1/3 ,1/2 )
对于Al:起点O(0,0),盐酸恰好完全反应时为C点(1/3 ,1/2 )
![]() 显然,当n<1/2 时,Na<Mg<Al
显然,当n<1/2 时,Na<Mg<Al
![]() 当 1/2≤n<1时,Na<Mg=Al
当 1/2≤n<1时,Na<Mg=Al
![]() 当n=1时,Na=Mg=Al
当n=1时,Na=Mg=Al
![]() 当n>1时,Na>Mg=Al.
当n>1时,Na>Mg=Al.

练习册系列答案
 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案
相关题目