题目内容
海洋中有丰富的食品、矿产、能源、药物和水产资源等(如图所示)下列有关说法正确的是(  )
)
 )
)| A、氯碱工业是指以电解烙融NaCl为基础取Cl2等产品的工业 |
| B、流程②中结晶出的MgCl2?6H2O可在空气中受热分解制无水MgCl2 |
| C、在流程③④⑤中溴元素均被氧化 |
| D、流程①中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的药品顺序为BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸 |
考点:海水资源及其综合利用
专题:
分析:A、工业上用电解饱和NaCl溶液的方法来制取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品,称为氯碱工业氯碱工业;
B、氯化镁中的镁离子能水解,酸性环境会抑制水解;
C、在氧化还原反应中,失电子化合价升高的元素被氧化;
D、除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可以加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除钙离子和过量的钡离子,盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,加氢氧化钠和氯化钡无先后顺序要求.
B、氯化镁中的镁离子能水解,酸性环境会抑制水解;
C、在氧化还原反应中,失电子化合价升高的元素被氧化;
D、除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可以加过量的氯化钡除去硫酸根离子,然后用碳酸钠去除钙离子和过量的钡离子,盐酸要放在最后,来除去过量的氢氧化钠和碳酸钠,加氢氧化钠和氯化钡无先后顺序要求.
解答:
解:A、工业上用电解饱和NaCl溶液的方法来制取NaOH、Cl2和H2,并以它们为原料生产一系列化工产品,称为氯碱工业氯碱工业,故A错误;
B、②中由MgCl2?6H2O制备无水MgCl2的过程需要在氯化氢气流中进行,防止镁离子水解,故B错误;
C、④中溴得电子化合价降低,所以溴元素被还原,故C错误;
D、镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以正确的顺序为NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸,或者BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸,故D正确;
故选:D.
B、②中由MgCl2?6H2O制备无水MgCl2的过程需要在氯化氢气流中进行,防止镁离子水解,故B错误;
C、④中溴得电子化合价降低,所以溴元素被还原,故C错误;
D、镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀,硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀,至于先除镁离子,还是先除硫酸根离子都行,钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀,但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡,离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,所以正确的顺序为NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸,或者BaCl2溶液→NaOH溶液→Na2CO3溶液→过滤后加盐酸,故D正确;
故选:D.
点评:本题考查了海水资源及其综合利用,难点是除杂过程中加入药品的先后顺序,要根据物质的特点来分析解答,难度中等.

练习册系列答案
相关题目
下列说法不正确的是( )
| A、用石灰石或石灰乳进行燃煤烟气脱硫(除SO2)可获得副产品石膏 |
| B、金属的电化学防护措施有牺牲阳极的阴极保护法和外加电流的阴极保护法 |
| C、若在水里贮藏室中,放几块被KMnO4溶液浸透过的“砖块”,可延长水果保存时间 |
| D、常温时,某可逆反应的平衡常数越大则其反应速率就越快 |
 常温下,向某浓度H2A溶液中逐滴加入一定量浓度NaOH溶液,所得溶液中H2A、HA-、A2-三种微粒的物质的量分数与溶液pH的关系如图所示,则下列说法中不正确的是( )
常温下,向某浓度H2A溶液中逐滴加入一定量浓度NaOH溶液,所得溶液中H2A、HA-、A2-三种微粒的物质的量分数与溶液pH的关系如图所示,则下列说法中不正确的是( )| A、H2A是一种二元弱酸 |
| B、常温下,H2A=H++HA-的电离平衡常数Ka1=0.01 |
| C、将相同物质的量的NaHA和Na2A固体溶于水所得混合溶液pH一定为5.5 |
| D、在量热计中,用20.0mL0.10mol/LnaOH溶液,分别与10.0mL0.20mol/LH2A和20.0mL0.10mol/LH2A反应后放出的热量不相同 |
下列图示的四种化学操作名称从左到右分别是( )
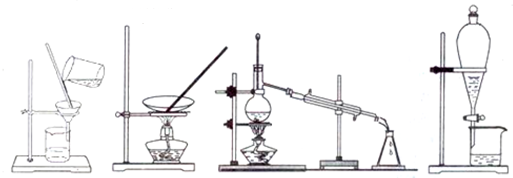

| A、蒸发、蒸馏、蒸发、过滤分液 |
| B、过滤、蒸馏、蒸发、萃取分液 |
| C、蒸发、蒸馏、过滤、萃取分液 |
| D、过滤、蒸发、蒸馏、萃取分液 |
 如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y,若挤压胶头滴管使液体滴入瓶中,振荡,一段时间后可见小球a?膨胀鼓起.下表中的各组物质不出现上述现象的是( )
如图所示,广口瓶中盛有气体X,胶头滴管中盛有液体Y,若挤压胶头滴管使液体滴入瓶中,振荡,一段时间后可见小球a?膨胀鼓起.下表中的各组物质不出现上述现象的是( )
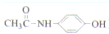 )(以下简称X)是最常用的非甾体消炎解热镇痛药,用于治疗感冒发烧和关节痛、神经痛、偏头痛等病症,它可用如下方法来合成
)(以下简称X)是最常用的非甾体消炎解热镇痛药,用于治疗感冒发烧和关节痛、神经痛、偏头痛等病症,它可用如下方法来合成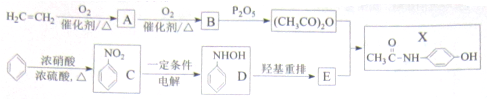
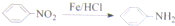 .请回答下列问题:
.请回答下列问题: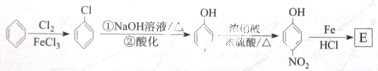
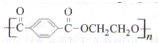 .请设计合成路线(无机试剂及溶剂任选)
.请设计合成路线(无机试剂及溶剂任选)