题目内容
17.下列物质在常温下发生水解时,对应的水解方程式正确的是( )| A. | K2CO3:CO${\;}_{3}^{2-}$+2H20?H2CO3+OH- | B. | Ca(ClO)2:ClO-+H2O=HClO+OH- | ||
| C. | Ba(HCO3)2:HCO3-+H2O?H3O++CO32- | D. | Na2SO3:SO32-+H2O?HSO3-+OH- |
分析 A.CO32-水解分步进行,以第一步水解为主;
B.水解反应为可逆反应;
C.水解生成碳酸和氢氧根离子;
D.SO32-水解分步进行,以第一步水解为主.
解答 解:A.水解离子反应为CO32-+H20?HCO3-+OH-,故A不选;
B.水解离子反应为ClO-+H2O?HClO+OH-,故B不选;
C.水解离子反应为HCO3-+H2O?H2CO3+OH-,故C不选;
D.Na2SO3的水解离子反应为SO32-+H2O?HSO3-+OH-,故D选;
故选D.
点评 本题考查水解离子反应方程式书写,为高频考点,把握水解规律及水解离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.在室温下,100ml 0.1mol/L的醋酸溶液中,欲使其溶液的pH值减小,但又要使醋酸电离程度减少,应采取( )
| A. | 加入少量CH3COONa固体 | B. | 通入少量氯化氢气体 | ||
| C. | 提高温度 | D. | 加入少量水 |
12.准确称取一定量纯净的H2C2O4•2H2O于锥形瓶中,加入适量的蒸馏水和稀硫酸,用未知浓度的高锰酸钾溶液进行滴定,从而标定高锰酸钾溶液的浓度.下列说法正确的是( )
| A. | KMnO4溶液可盛放在碱式滴定管中 | |
| B. | 可用酚酞或甲基橙作滴定的指示剂 | |
| C. | 若滴定管未用待测KMnO4溶液润洗,则会使测得的KMnO4溶液浓度偏小 | |
| D. | 滴定过程中褪色速率先慢后快,是由于锥形瓶中KMnO4溶液浓度不断增大 |
某同学体检的血液化验单中,出现了如下图所示的体检指标。表示该体检指标的物理量是
甘油三酯 | 0.52 | mmol/L |
总胆固醇 | 4.27 | mmol/L |
高密度脂蛋白胆固醇 | 1.57 | mmol/L |
低密度脂蛋白胆固醇 | 1.40 | mmol/L |
葡萄糖 | 4.95 | mmol/L |
A.溶解度 B.物质的量浓度 C.质量分数 D.摩尔质量
16.下列关于电离平衡常数(K)的说法中正确的是( )
| A. | 在一定温度,相同浓度时电离平衡常数(K)越大可以表示弱电解质电离程度越大 | |
| B. | 电离平衡常数(K)与温度无关 | |
| C. | 不同浓度的同一弱电解质,其电离平衡常数(K)不同 | |
| D. | 多元弱酸各步电离平衡常数相互关系为K1<K2<K3 |
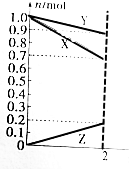 某温度时,在2L的容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示.由图中数据分析:该反应的化学方程式为Y+3X=2Z.反应开始至2min,用Z表示的平均反应速率为0.05mol/(L.min).
某温度时,在2L的容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示.由图中数据分析:该反应的化学方程式为Y+3X=2Z.反应开始至2min,用Z表示的平均反应速率为0.05mol/(L.min).