题目内容
20.短周期元素X、Y、Z、W、Q在元素周期表中的位置如图所示,Z元素的简单离子半径在本周期中最小,下列说法不正确的是( )| X | Y | |||
| z | W | Q |
| A. | Y元素气态氢化物的稳定性大于X元素的气态氢化物 | |
| B. | 形成的简单离子半径:W>Q>Z>X | |
| C. | Q的最高价氧化物对应的水化物酸性最强 | |
| D. | X的最高价氧化物对应的水化物与其氢化物形成的化合物中含有离子键和共价键 |
分析 由短周期元素X、Y、Z、W、Q在元素周期表中的位置,可知X、Y处于第二周期,Z、W、Q处于第三周期,Z元素的简单离子半径在本周期中最小,则Z为Al,可推知X为N、Y为、W为S、Q为Cl.
A.同周期自左而右元素非金属性增强,氢化物稳定性增强;
B.电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大;
C.最高价氧化物对应水化物中高氯酸的酸性最强;
D.X的最高价氧化物对应的水化物与其氢化物形成的化合物为NH4NO3,含有离子键和共价键.
解答 解:由短周期元素X、Y、Z、W、Q在元素周期表中的位置,可知X、Y处于第二周期,Z、W、Q处于第三周期,Z元素的简单离子半径在本周期中最小,则Z为Al,可推知X为N、Y为、W为S、Q为Cl.
A.非金属性Y(O)>X(N),故氢化物稳定性:Y>X,故A正确;
B.电子层结构相同的离子,核电荷数越大离子半径越小,离子电子层越多离子半径越大,故离子半径:S2->Cl->N3->Na+,故B错误;
C.Q的最高价氧化物对应的水化物为高氯酸,其酸性最强,故C正确;
D.X的最高价氧化物对应的水化物与其氢化物形成的化合物为NH4NO3,含有离子键和共价键,故D正确.
故选:B.
点评 本题考查结构性质位置关系应用,关键是掌握离子半径大小比较,熟练掌握元素周期表的结构与元素周期律.

练习册系列答案
相关题目
10.下列实验操作能达到目的是( )
| A. | 用加热蒸发K2CO3溶液的方法获得K2CO3晶体 | |
| B. | 用Na2S溶液和Al2(SO4)3溶液反应制取Al2S3固体 | |
| C. | 用Na2S溶液和CuSO4溶液反应无法制取CuS固体 | |
| D. | 加热MgCl2溶液制取MgCl2固体 |
11.反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,下列说法正确的是( )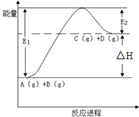

| A. | 该反应是放热反应 | |
| B. | 加入催化剂后,反应加快,△H减小 | |
| C. | 反应物的总键能小于生成物的总键能 | |
| D. | 反应达到平衡时,升高温度,A的转化率增大 |
15.下列物质中,属于共价化合物的是( )
| A. | NaCl | B. | Na2O | C. | Cl2 | D. | CO2 |
5.下表是元素周期表的一部分,回答下列问题:
(1)在这些元素中,F(用元素符号填写,下同)是最活泼的非金属元素;Ar是最不活泼的元素.
(2)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;能形成两性氢氧化物的元素是Al.
(3)从⑤到⑪的元素中,Cl原子半径最小,写出③形成的氢化物的电子式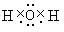 .
.
(4)⑥、⑩的最高价氧化物分别属于离子、共价型化合物(填离子,共价)
(5)比较⑤与⑥的化学性质,钠更活泼,试用实验证明(简述简单操作、主要现象和结论)取少量金属钠和金属镁,都投入冷水中,金属钠和冷水剧烈反应,生成无色气体,钠迅速消失. 而镁和冷水几乎不反应,无明显现象,证明了金属钠比金属镁活泼.
| 周期/族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ○ |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ⑫ |
(2)这些元素的最高价氧化物的对应水化物中HClO4酸性最强;能形成两性氢氧化物的元素是Al.
(3)从⑤到⑪的元素中,Cl原子半径最小,写出③形成的氢化物的电子式
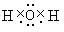 .
.(4)⑥、⑩的最高价氧化物分别属于离子、共价型化合物(填离子,共价)
(5)比较⑤与⑥的化学性质,钠更活泼,试用实验证明(简述简单操作、主要现象和结论)取少量金属钠和金属镁,都投入冷水中,金属钠和冷水剧烈反应,生成无色气体,钠迅速消失. 而镁和冷水几乎不反应,无明显现象,证明了金属钠比金属镁活泼.
12.已知括号中为杂质,则下列除杂试剂正确的是( )
| A. | 丙烷(丙烯),酸性高锰酸钾溶液 | B. | 甲烷(乙炔),溴的四氯化碳溶液 | ||
| C. | 溴苯(溴),苯 | D. | 硝基苯(硝酸),苯和浓硫酸 |
9.设NA为阿伏伽德罗常数的值,下列叙述不正确的是( )
| A. | 1molNa与O2完全反应生成Na2O2和Na2O的混合物,转移电子的总数为NA | |
| B. | 室温下,31.0g白磷中含有的共价键数目为1.5NA | |
| C. | 常温常压下,17g甲基(-14CH3)含有的电子数为9NA | |
| D. | 常温下,1.0L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA |
12.金属钛(Ti)被誉为21世纪金属,具有良好的生物相容性,它兼具铁的高强度和铝的低密度.其单质和化合物具有广泛的应用价值.氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品.以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2(如图1).
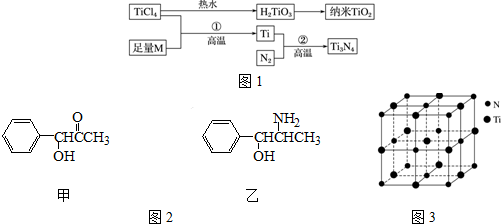
图中的M是短周期金属元素,M的部分电离能如表:请回答下列问题:
(1)Ti的基态原子外围电子排布式为4d25s2;
(2)M是Mg(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为12;
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C;
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$ g•cm-3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个;
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如下:
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为TiN>CaO>KCl.

图中的M是短周期金属元素,M的部分电离能如表:请回答下列问题:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/kJ•mol-1 | 738 | 1451 | 7733 | 1054 0 | 13630 |
(2)M是Mg(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为12;
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C;
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$ g•cm-3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个;
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如下:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |