题目内容
(13分)实验室用乙酸和正丁醇制备乙酸正丁酯。有关物质的相关数据如下表:
化合物 | 相对分子质量 | 密度/g·cm-3 | 沸点,/℃ | 溶解度/l00g水 |
正丁醇 | 74 | 0.80 | 118.0 | 9 |
冰醋酸 | 60 | 1.045 | 118.1 | 互溶 |
乙酸正丁酯 | 116 | 0.882 | 126.1 | 0.7 |
操作如下:
①在50mL三颈烧瓶中,加入18.5 mL正丁醇和13.4 mL冰醋酸, 3~4滴浓硫酸,投入沸石。安装分水器(作用:实验过程中不断分离除去反应生成的水)、温度计及回流冷凝管。
②将分水器分出的酯层和反应液一起倒入分液漏斗中,水洗, 10% Na2CO3洗涤,再水洗,最后转移至锥形瓶,干燥。
③将干燥后的乙酸正丁酯滤入烧瓶中,常压蒸馏,收集馏分,得15.1 g乙酸正丁酯。

请回答有关问题:
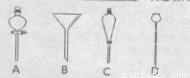
(1)冷水应该从冷凝管 (填a或b)端管口通入。
(2)仪器A中发生反应的化学方程式为____ 。
(3)步骤①“不断分离除去反应生成的水”该操作的目的是: 。
(4)步骤②中用10%Na2CO3溶液洗涤有机层,该步操作的目的是 。
(5)进行分液操作时,使用的漏斗是____ (填选项)。
(6)步骤③在进行蒸馏操作时,若从118℃开始收集馏分,产率偏___ (填“高”或者“低”)原因是____
(7)该实验过程中,生成乙酸正丁酯的产率是 。
(1)a(1分)
(2)CH3COOH+CH3CH2CH2CH2OH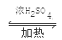 CH3COOCH2CH2CH2CH3+H2O(2分)
CH3COOCH2CH2CH2CH3+H2O(2分)
(3)使用分水器分离出水,使平衡正向移动,提高反应产率(2分);
(4)除去产品中含有的乙酸等杂质(2分)
(5)C(1分)
(6)高(1分) 会收集到少量未反应的冰醋酸和正丁醇(2分)
(7)65% (2分)
【解析】
试题分析:(1)为了增强水的冷凝效果,冷水应该从冷凝管从下口a端管口通入。(2)在仪器A中乙酸与正丁醇在浓硫酸作用下发生酯化反应产生乙酸正丁酯和水,发生反应的化学方程式为CH3COOH+CH3CH2CH2CH2OH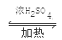 CH3COOCH2CH2CH2CH3+H2O ;(3)步骤①“不断分离除去反应生成的水”是因为该反应是可逆反应,减小生成物水的浓度,可以使该平衡正向移动,提高反应产率;(4)步骤②中得到的酯中含有未完全反应的挥发出的乙酸,用10%Na2CO3溶液洗涤有机层,该步操作的目的就是除去产品中含有的乙酸等杂质;(5)进行分液操作时,使用的漏斗是分液漏斗AC.但是A的容积小,不利于物质的充分分离,所以应该选择C;(6)由于正丁醇的沸点是118.0,乙酸的沸点是118.1,所以在步骤③在进行蒸馏操作时,若从118℃开始收集馏分,正丁醇和乙酸也混在其中,使得收集的产物质量偏多,所以产率偏高;(7)乙酸正丁酯的物质的量是15.1 g÷116g/mol=0.13mol;n(乙酸)=(13.4 mL×1.045g/ml)÷60g/mol=0.23mol>n(正丁醇)=(0.80g/ml×18.5 mL)÷74g/mol=0.2mol,所以反应产生的酯应该按照醇来计算,该实验过程中,生成乙酸正丁酯的产率是(0.13mol÷0.20mol)×100%=65%。
CH3COOCH2CH2CH2CH3+H2O ;(3)步骤①“不断分离除去反应生成的水”是因为该反应是可逆反应,减小生成物水的浓度,可以使该平衡正向移动,提高反应产率;(4)步骤②中得到的酯中含有未完全反应的挥发出的乙酸,用10%Na2CO3溶液洗涤有机层,该步操作的目的就是除去产品中含有的乙酸等杂质;(5)进行分液操作时,使用的漏斗是分液漏斗AC.但是A的容积小,不利于物质的充分分离,所以应该选择C;(6)由于正丁醇的沸点是118.0,乙酸的沸点是118.1,所以在步骤③在进行蒸馏操作时,若从118℃开始收集馏分,正丁醇和乙酸也混在其中,使得收集的产物质量偏多,所以产率偏高;(7)乙酸正丁酯的物质的量是15.1 g÷116g/mol=0.13mol;n(乙酸)=(13.4 mL×1.045g/ml)÷60g/mol=0.23mol>n(正丁醇)=(0.80g/ml×18.5 mL)÷74g/mol=0.2mol,所以反应产生的酯应该按照醇来计算,该实验过程中,生成乙酸正丁酯的产率是(0.13mol÷0.20mol)×100%=65%。
考点:考查实验室制取酯的反应原理、仪器的使用、操作、混合物的分离和物质产率的计算的知识。

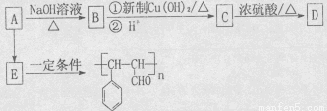
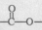 的芳香族化合物的同分异构体有___ _种,写出其中核磁共振氢谱有4个峰的一种结构简式 。
的芳香族化合物的同分异构体有___ _种,写出其中核磁共振氢谱有4个峰的一种结构简式 。 由甲苯及其它必要物质经如下步骤也可合成B:
由甲苯及其它必要物质经如下步骤也可合成B: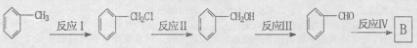
 HSO3-+OH-水解平衡的事实是 (填选项字母)。
HSO3-+OH-水解平衡的事实是 (填选项字母)。 C(g)+3D(s),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:Ⅰ. A、B的起始物质的量均为2 mol,Ⅱ.C、D的起始物质的量分别为2 mol和6 mol。以下说法中正确的是 (填选项字母)。
C(g)+3D(s),在密闭容器的容积、温度都相同的条件下,分别从以下两条途径建立平衡:Ⅰ. A、B的起始物质的量均为2 mol,Ⅱ.C、D的起始物质的量分别为2 mol和6 mol。以下说法中正确的是 (填选项字母)。