题目内容
13.高温下,某反应平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$.恒容条件下达到平衡时,温度升高H2浓度减小.下列说法正确的是( )| A. | 该反应的化学方程式为CO+H2O$?_{高温高压}^{催化剂}$CO2+H2 | |
| B. | 该反应的焓变为正值 | |
| C. | 恒温恒容下,增大压强,H2浓度一定减小 | |
| D. | 升高温度,平衡右移,逆反应速率减小 |
分析 A.K为生成物浓度幂之积与反应物浓度幂之积的比;
B.由K可知,氢气为反应物,温度升高H2浓度减小,可知升高温度,平衡正向移动;
C.恒温恒容时,增大压强,pV=nRT可知,气体的物质的量可能增大;
D.升高温度,反应速率增大,平衡向吸热的方向移动.
解答 解:A.由平衡常数K=$\frac{c(CO)•c({H}_{2}O)}{c(C{O}_{2})•c({H}_{2})}$,可知该反应的化学方程式CO2(g)+H2(g)?CO(g)+H2O(g),故A错误;
B.温度升高时H2浓度减小,说明在升温时平衡正向移动,△H>0,故B正确;
C.恒容增大压强的方式不确定,所以H2的浓度变化不确定,故C错误;
D.升高温度,平衡右移,但v正和v逆都增大,故D错误;
故选B.
点评 本题考查平衡常数的意义及化学平衡移动,为高频考点,把握温度、压强对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意K与反应的关系,题目难度不大.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
9.对于反应8NH3+3Cl2═N2+6NH4Cl,下列说法正确的是( )
| A. | N2是还原产物,且还原剂与氧化剂物质的量之比是2:3 | |
| B. | N2是氧化产物,且还原剂与氧化剂物质的量之比是2:3 | |
| C. | 每转移6mol电子就生成22.4LN2 | |
| D. | NH4Cl是氧化产物,且还原产物与氧化产物物质的量之比是1:6 |
4.25℃时,电离常数Ka(HF)=3.6×10-4mol/L,溶度积Ksp(CaF2)=1.46×10-10,Ksp(AgCl)=4×10-10,Ksp(AgI)=1.0×10-16.下列说法正确的是( )
| A. | AgCl不能转化为AgI | |
| B. | 25℃时,0.1mol/L HF溶液pH=l | |
| C. | 25℃时,使AgCl转化为AgI,则加入KI溶液的浓度不低于5×10-12mol/L | |
| D. | 向1L0.1mol/LHF溶液中加入1L 0.1mol/LCaCl2溶液,没有沉淀产生 |
1.镍氢电池是近年开发出来的可充电电池,它可以取代会产生镉污染的镉镍电池.镍氢电池的总反应式是:H2+2NiO(OH) $?_{充电}^{放电}$ 2Ni(OH)2,据此反应判断,下列叙述中正确的是( )
| A. | 电池放电时,电池负极周围溶液的pH 不断增大 | |
| B. | 电池充电时,阳极反应为:Ni(OH)2+OH--e-═NiO(OH)+H2O | |
| C. | 电池充电时,氢元素被氧化 | |
| D. | 电池放电时,负极反应为:H2-2e-═2H+ |
8.在同温同压下,分子数相同的任意两种气体,它们的( )
| A. | 体积都是22.4L | B. | 密度相同 | C. | 所占体积相同 | D. | 原子数目相同 |
18.下列离子方程式书写正确的是( )
| A. | 铁与硫酸铜溶液反应:Fe+Cu2+═Fe2++Cu | |
| B. | 氧化镁与稀盐酸混合:MgO+H+═Mg2++H2O | |
| C. | 碳酸钙与盐酸反应:CO32-+2H+═CO2↑+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO42-═BaSO4↓ |
2.对下列物质的类别与所含官能团的分析判断中,不正确的是( )
| A. | 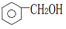 醇类-OH 醇类-OH | B. | CH3CH2COOH 羧酸类-COOH | ||
| C. | 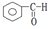 酮类-CHO 酮类-CHO | D. | CH3CH2Br 卤代烃类-Br |
3.食盐,食醋,纯碱(Na2CO3)均为家庭厨房中常用的物质,利用这些物质不能完成的实验是( )
| A. | 检验自来水中是否含Cl- | B. | 检验鸡蛋壳(CaCO3)能否溶于酸 | ||
| C. | 鉴别AgNO3 溶液和BaCl2 溶液 | D. | 除去热水瓶内壁上的水垢 |