题目内容
15.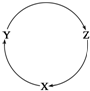 下列各组物质中,不能满足下图物质一步转化关系的选项是( )
下列各组物质中,不能满足下图物质一步转化关系的选项是( )| 选项 | X | Y | Z |
| A | NaOH | Na2CO3 | NaHCO3 |
| B | C | CO | CO2 |
| C | Cu | CuSO4 | Cu(OH)2 |
| D | AlCl3 | NaAlO2 | Al(OH)3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.NaOH和二氧化碳反应生成Na2CO3,Na2CO3和二氧化碳反应生成碳酸氢钠,碳酸氢钠与氢氧化钙反应生成NaOH;
B.C不完全燃烧得到CO,CO与氧气反应得到CO2,CO2与Mg反应可以得到C;
C.Cu与浓硫酸反应生成硫酸铜,硫酸铜和氢氧化钠反应生成Cu(OH)2,Cu(OH)2不能直接生成Cu;
D.AlCl3与过量NaOH反应生成NaAlO2,NaAlO2与二氧化碳反应生成Al(OH)3,Al(OH)3与盐酸反应生成AlCl3.
解答 解:A.NaOH和二氧化碳反应生成Na2CO3和水,向Na2CO3溶液中通入二氧化碳,碳酸钠与二氧化碳、水反应生成碳酸氢钠,碳酸氢钠与过量的氢氧化钙溶液反应生成NaOH和碳酸钙沉淀,所以能实现一步转化,故A不选;
B.C不完全燃烧得到CO,CO与氧气反应得到CO2,Mg在二氧化碳中燃烧生成C和MgO,则CO2与Mg反应可以得到C,所以能实现一步转化,故B不选;
C.Cu与浓硫酸在加热条件下反应生成硫酸铜,硫酸铜和氢氧化钠溶液反应生成Cu(OH)2和硫酸钠,Cu(OH)2不能直接生成Cu,所以不能实现一步转化,故C选;
D.AlCl3与过量NaOH溶液反应生成NaAlO2和水,在NaAlO2溶液中通入二氧化碳,会发生反应生成Al(OH)3沉淀,Al(OH)3与盐酸反应生成AlCl3和水,所以能实现一步转化,故D不选;
故选C.
点评 本题考查物质之间的转化,侧重考查元素化合物知识,明确物质的性质是解本题关键,题目难度不大,侧重于考查学生对基础知识的应用能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列有关物质的检验或区分方法中不正确的是( )
| A. | 向某溶液中加入BaCl2溶液,有白色沉淀,则原溶液一定存在Ag+或SO42- | |
| B. | 根据纤维在火焰上燃烧产生的气味,可确定该纤维是否为蛋白质纤维 | |
| C. | 两份常温下均为饱和溶液(一份是NaOH溶液,一份是氢氧化钙溶液),上述两份饱和溶液可通过加入少量的NaOH固体而鉴别出 | |
| D. | 某矿石中加入足量的盐酸,根据放出的二氧化碳气体,可证明该矿石一定含有碳酸盐 |
4.下列物质中属于弱电解质的是( )
| A. | 醋酸 | B. | 氨 | C. | 碳酸氢钠 | D. | NaOH溶液 |
5.下列过程有热量放出的是( )
| A. | 断开氢气中的H-H键 | B. | Ba(OH)2•8H2O晶体与NH4Cl晶体反应 | ||
| C. | C与H2O(g)反应 | D. | Na与H2O反应 |
 和
和