题目内容
7.下列与有机物的结构、性质有关的叙述正确的是( )| A. | 苯、油脂均不能使酸性KMnO4溶液褪色 | |
| B. | 甲烷和Cl2的反应与乙烯和Br2的反应属于同一类型的反应 | |
| C. | 葡萄糖、果糖的分子式均为C6H12O6,二者互为同分异构体 | |
| D. | 除去乙酸乙酯中的乙酸,先加入饱和Na2CO3溶液再分液 |
分析 A.苯中不含碳碳双键、油脂含碳碳双键;
B.甲烷和Cl2的反应为取代反应,乙烯和Br2的反应为加成反应;
C.二者均为单糖,分子式相同、结构不同;
D.乙酸与碳酸钠反应后,与乙酸乙酯分层.
解答 解:A.苯中不含碳碳双键、油脂含碳碳双键,则油脂能使酸性KMnO4溶液褪色,故A错误;
B.甲烷和Cl2的反应为取代反应,乙烯和Br2的反应为加成反应,二者反应类型不同,故B错误;
C.二者均为单糖,分子式相同、结构不同,二者互为同分异构体,故C正确;
D.乙酸与碳酸钠反应后,与乙酸乙酯分层,然后分液可分离,故D正确.
故选CD.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团、性质、有机反应为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
12.设NA为阿伏加德罗常数,下列叙述中正确的是( )
| A. | 标准状况下,22.4L H2中所含质子数、中子数均为2NA | |
| B. | 32g O2气体和32g O3气体的分子数之比为3:2 | |
| C. | 1L 1mol•L-1的盐酸中所含粒子总数为2NA | |
| D. | 71g氯气与足量铁粉充分反应,转移的电子数为3NA |
2.碘酸钾是一种白色结晶粉末,无臭无味,酸性条件下碘酸钾是一种较强的氧化剂,与氢碘酸、二氧化硫等还原性物质作用,被还原为单质碘,在碱性介质中,碘酸钾能被氯气、次氯酸盐等氧化为高碘酸钾.碘酸钾在常温下稳定,加热至560℃开始分解.工业生产碘酸钾的流程如下,在反应器中发生反应的化学方程式为:I2+KClO3+H2O→KH(IO3)2+KCl+Cl2↑(未配平)
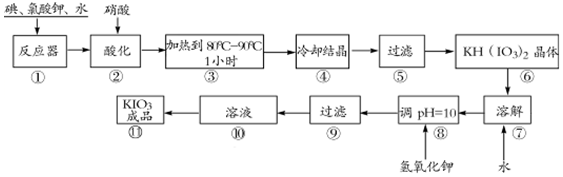
(1)已知步骤①反应器发生的反应中,两种还原产物所得电子数相同,请配平该反应的化学方程式:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑;
(2)步骤②中,用稀酸酸化的作用是促进氯气从反应混合物中逸出;
(3)步骤③要保持溶液微沸1小时以完全排出氯气,排出氯气的原因为Cl2能将KIO3氧化成KIO4;
(4)参照下表碘酸钾的溶解度,步骤11得到碘酸钾晶体,你建议的方法是蒸发浓缩、冷却结晶.

(1)已知步骤①反应器发生的反应中,两种还原产物所得电子数相同,请配平该反应的化学方程式:6I2+11KClO3+3H2O=6KH(IO3)2+5KCl+3Cl2↑;
(2)步骤②中,用稀酸酸化的作用是促进氯气从反应混合物中逸出;
(3)步骤③要保持溶液微沸1小时以完全排出氯气,排出氯气的原因为Cl2能将KIO3氧化成KIO4;
(4)参照下表碘酸钾的溶解度,步骤11得到碘酸钾晶体,你建议的方法是蒸发浓缩、冷却结晶.
| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 |
| KIO3g/100g水 | 4.60 | 6.27 | 8.08 | 12.6 | 18.3 | 24.8 |
19.误食NaNO2会导致血红蛋白中的Fe2+氧化为Fe3+而中毒,服用维生素C可以解除NaNO2引起的中毒.下列关于上述中毒、解毒过程的说法中正确的是( )
| A. | NaNO2是还原剂 | |
| B. | 维生素C的还原性强于Fe2+ | |
| C. | 1×10-3molFe2+被NaNO2氧化为Fe3+时得到1×10-3mol电子 | |
| D. | 解毒过程中维生素C被还原 |
16.鲨鱼体内含有的角鲨烯具有抗癌性.实验测得角鲨烯分子是链状结构,分子中含有30个碳原子且碳氢质量比为7.2:1,下列说法不正确的是( )
| A. | 角鲨烯分子式为C30H50 | |
| B. | 角鲨烯可以被酸性KMnO4溶液所氧化 | |
| C. | 1mol角鲨烯最多可与6molH2发生加成反应 | |
| D. | 汽油经过催化裂化可以获得角鲨烯 |
17.下列物质属于电解质的是( )
| A. | 氯水 | B. | Cu | C. | NH3 | D. | CaO |
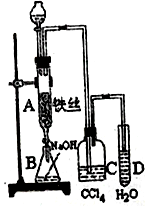 某学生在如图所示的装置中用苯和液溴制取溴苯,请根据下列实验步骤回答有关问题.
某学生在如图所示的装置中用苯和液溴制取溴苯,请根据下列实验步骤回答有关问题. ;
;