题目内容
下列离子方程式正确的是( )
| A、三氯化铝溶液中加入过量氨水:Al3++3OH-═Al(OH)3↓ | ||||
| B、向含有0.2 mol FeI2的溶液中通入0.25 mol Cl2:8I-+2Fe2++5Cl2═10Cl-+4I2+2Fe3+ | ||||
C、K37ClO3与浓盐酸(HCl)在加热时生成Cl2:37ClO3-+6HCl
| ||||
| D、将0.1 mol/L盐酸数滴缓缓滴入0.1 mol/L 25 mL Na2CO3溶液中,并不断搅拌:2H++CO32-═CO2↑+H2O |
考点:离子方程式的书写
专题:
分析:A.一水合氨在离子反应中保留化学式,反应生成氢氧化铝和氯化铵;
B.还原性碘离子大于亚铁离子,氯气得到电子为0.25mol×2×1=0.5mol,由电子守恒可知,碘离子全部被氧化,亚铁离子一半被氧化;
C.氯酸钾为氧化剂,对应还原产物为氯气;
D.盐酸数滴缓缓滴入碳酸钠溶液中,盐酸不足,生成碳酸氢钠.
B.还原性碘离子大于亚铁离子,氯气得到电子为0.25mol×2×1=0.5mol,由电子守恒可知,碘离子全部被氧化,亚铁离子一半被氧化;
C.氯酸钾为氧化剂,对应还原产物为氯气;
D.盐酸数滴缓缓滴入碳酸钠溶液中,盐酸不足,生成碳酸氢钠.
解答:
解:A.三氯化铝溶液中加入过量氨水的离子反应为Al3++3NH3.H2O═Al(OH)3↓+3NH4+,故A错误;
B.向含有0.2 mol FeI2的溶液中通入0.25 mol Cl2的离子反应为8I-+2Fe2++5Cl2═10Cl-+4I2+2Fe3+,故B正确;
C.K37ClO3与浓盐酸(HCl)在加热时生成Cl2的离子反应为237ClO3-+12H++10Cl-
37Cl2↑+5Cl2↑+6H2O,故C错误;
D.将0.1 mol/L盐酸数滴缓缓滴入0.1 mol/L 25 mL Na2CO3溶液中,并不断搅拌的离子反应为H++CO32-═HCO3-,故D错误;
故选B.
B.向含有0.2 mol FeI2的溶液中通入0.25 mol Cl2的离子反应为8I-+2Fe2++5Cl2═10Cl-+4I2+2Fe3+,故B正确;
C.K37ClO3与浓盐酸(HCl)在加热时生成Cl2的离子反应为237ClO3-+12H++10Cl-
| ||
D.将0.1 mol/L盐酸数滴缓缓滴入0.1 mol/L 25 mL Na2CO3溶液中,并不断搅拌的离子反应为H++CO32-═HCO3-,故D错误;
故选B.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解及氧化还原反应的离子反应考查,题目难度不大.

练习册系列答案
相关题目
下列实验能达到目的是( )
| A、将NH4Cl溶液蒸干制备NH4Cl固体 |
| B、只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液 |
| C、用萃取分液的方法除去酒精中的水 |
| D、用可见光束照射以区别溶液和胶体 |
溶液、胶体和浊液这三种分散系的根本区别是( )
| A、是否能产生丁达尔效应 |
| B、分散质粒子直径的大小 |
| C、分散质粒子能否透过滤纸 |
| D、是否均一、稳定、透明 |
下列关于分散系的说法,正确的是( )
| A、混合物都属于分散系 |
| B、稀豆浆中分散质粒子的直径在1-100nm |
| C、FeCl3溶液中分散质的粒子为FeCl3 |
| D、含有1 mol FeCl3的饱和溶液加入到沸水中生成1 molFe(OH)3胶粒 |
下列有关物质的表达式不正确的是( )
| A、乙烯的最简式:C2H4 |
| B、CS2分子的结构式:S═C═S |
| C、醛基的结构简式:-CHO |
D、-OH(羟基)的电子式为: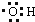 |
下列物质中,没有固定沸点的是( )
| A、聚乙烯 | B、氯仿 |
| C、甲苯 | D、异丁烷 |