题目内容
下列变化(现象)的原理相同的是( )
| A、浓硫酸和浓盐酸敞口存放浓度均变小 |
| B、将单质铁和铜分别与单质硫加热反应均生成低价硫化物(FeS和Cu2S) |
| C、在过氧化氢水溶液中加入二氧化锰、在盛有锌粒和稀硫酸的溶液中滴加硫酸铜溶液,产生气体的速率均加快 |
| D、将氯化铝溶液和碳酸氢钠溶液分别用酒精灯加热蒸干,然后灼烧,最后均得到白色固体 |
考点:化学试剂的存放,盐类水解的应用,过氧化氢,钠的重要化合物,铁的化学性质,铜金属及其重要化合物的主要性质
专题:
分析:A.浓硫酸具有吸水性,浓盐酸具有挥发性;
B.根据反应实质判断反应原理;
C.前者为催化剂加快反应速率,后者为形成原电池反应;
D.氯化铝水解,碳酸氢钠受热分解.
B.根据反应实质判断反应原理;
C.前者为催化剂加快反应速率,后者为形成原电池反应;
D.氯化铝水解,碳酸氢钠受热分解.
解答:
解:A.浓硫酸和浓盐酸在空气中敞口放置时浓度均减小,前者是因为浓硫酸的吸水性,后者是因为浓盐酸的挥发性,变化的实质不同,故A不选;
B.S与金属反应生成相应的硫化物,由于S的氧化性不是很强,与变价金属反应时生成金属低价态硫化物,故B选;
C.在过氧化氢水溶液中加入二氧化锰,二氧化锰起催化作用,反应速率加快,在盛有锌粒和稀硫酸的溶液中滴加硫酸铜溶液,锌把铜置换出来,形成铜锌原电池,加快反应速率,原理不同,故C不选;
D.氯化铝水解生成氢氧化铝和氯化氢,蒸干灼烧最后得到氧化铝,碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,二者原理不同,故D不选;
故选B.
B.S与金属反应生成相应的硫化物,由于S的氧化性不是很强,与变价金属反应时生成金属低价态硫化物,故B选;
C.在过氧化氢水溶液中加入二氧化锰,二氧化锰起催化作用,反应速率加快,在盛有锌粒和稀硫酸的溶液中滴加硫酸铜溶液,锌把铜置换出来,形成铜锌原电池,加快反应速率,原理不同,故C不选;
D.氯化铝水解生成氢氧化铝和氯化氢,蒸干灼烧最后得到氧化铝,碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,二者原理不同,故D不选;
故选B.
点评:根据反应实质判断反应原理.中等难度.注意S的氧化性不是很强,与变价金属反应时生成金属低价态硫化物,氯气具有强氧化性,与变价金属反应时生成金属高价态化合物.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案 口算心算速算应用题系列答案
口算心算速算应用题系列答案
相关题目
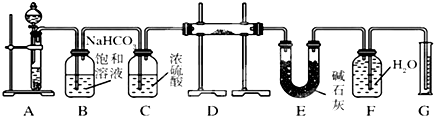
为测定石灰石样品中碳酸钙(含SiO2杂质)的含量.现利用如图所示装置进行实验,充分反应后,测定装置C中生成的BaCO3沉淀质量.下列说法正确的是( )


| A、装置A中药品应为浓硫酸 |
| B、在B-C之间应增添盛有饱和NaHCO3溶液的洗气装置,以除去氯化氢气体 |
| C、为了测得C中生成的沉淀质量,需经过过滤、洗涤、干燥、称量等操作 |
| D、只要测定装置C在吸收CO2前后的质量差,也可以确定碳酸钙的质量分数 |
下列叙述错误的是( )
| A、加热能杀死流感病毒是因为病毒的蛋白质受热变性 |
| B、人造纤维、含成纤维和光导纤维都是有机高分子化合物 |
| C、在汽车排气管上加装“催化转化器”怒为了减少有害气体的排放 |
| D、明矾[KAl(SO4)2?12H2O]在水中能形成Al(OH)3胶体,可用作净水剂 |
下列叙述错误的是( )
①糯米中的淀粉一经发生水解反应,就生成酒精
②蛋白质“溶液”是一种胶体,向该分散系中加入少量的盐(如硫酸铵)能促进蛋白质的溶解
③纤维素属于天然高分子化合物,一切植物均含有纤维素
④石油裂化的主要目的是为了生产乙烯、丙烯等有机化工原料
⑤乙醇在一定条件下可被氧化为乙醛.
①糯米中的淀粉一经发生水解反应,就生成酒精
②蛋白质“溶液”是一种胶体,向该分散系中加入少量的盐(如硫酸铵)能促进蛋白质的溶解
③纤维素属于天然高分子化合物,一切植物均含有纤维素
④石油裂化的主要目的是为了生产乙烯、丙烯等有机化工原料
⑤乙醇在一定条件下可被氧化为乙醛.
| A、④⑤ | B、②③ | C、①④ | D、①②④ |
下列过程中所发生的化学反应不属于取代反应的是( )
| A、光照射甲烷与氯气的混合气体 |
| B、在镍作催化剂的条件下,苯与氢气反应 |
| C、乙醇与乙酸在浓硫酸作用下加热 |
| D、苯与液溴混合后撒入铁粉 |
环境污染已成为人类社会面临的重大威胁,下列名词与环境污染有关的是( )
(1)酸雨 (2)臭氧空洞 (3)白色污染 (4)温室效应 (5)赤潮 (6)光化学烟雾.
(1)酸雨 (2)臭氧空洞 (3)白色污染 (4)温室效应 (5)赤潮 (6)光化学烟雾.
| A、只有(1)(3)(4)(5) |
| B、只有(1)(2)(3)(4)(6) |
| C、只有(3)(4)(5)(6) |
| D、全部 |
 阅读下列实验内容,根据题目要求回答问题.
阅读下列实验内容,根据题目要求回答问题.