题目内容
已知如表元素的原子半径:
根据表中数据,磷元素的原子半径可能是( )
| 元素 | N | S | O | Si |
| 原子半径/10-10m | 0.75 | 1.02 | 0.74 | 1.17 |
| A、0.80×10-10m |
| B、1.10×10-10m |
| C、1.20×10-1 m |
| D、0.70×10-10m |
考点:微粒半径大小的比较
专题:
分析:同周期自左而右原子半径减小,同主族自上而下原子半径增大.
解答:
解:N、P是同一主族元素,P元素的原子序数大于N元素的原子序数,所以原子半径:r(P)>0.75×10-10m;
Si、P、S是同一周期的元素,且P的原子序数大于Si的原子序数小于S的原子序数,所以原子半径:1.02×10-10m<r(P)<1.17×10-10m,
故磷元素的原子半径可能为1.10×10-10m,
故选B.
Si、P、S是同一周期的元素,且P的原子序数大于Si的原子序数小于S的原子序数,所以原子半径:1.02×10-10m<r(P)<1.17×10-10m,
故磷元素的原子半径可能为1.10×10-10m,
故选B.
点评:本题考查了微粒半径大小的比较,难度不大,注意电子层结构相同的离子半径大小的比较方法.

练习册系列答案
相关题目
大理石是一种重要的化工原料,其主要成分可以反应生成一系列物质,如下图所示.
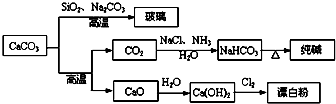
下列说法正确的是( )

下列说法正确的是( )
| A、Cl2和SO2均可以漂白有色物质,且漂白的原理相同 | ||||
B、由SiO2+Na2CO3
| ||||
| C、向饱和碳酸钠溶液中通入过量CO2,溶液变浑浊 | ||||
| D、制取玻璃和漂白粉所涉及的反应都是非氧化还原反应 |
下列物质中含有非极性共价键的离子化合物是( )
| A、Ba(OH)2 |
| B、CaCl2 |
| C、H2O |
| D、Na2O2 |
下列微粒中,中子数和质子数相等的是( )
①18O;②12C;③26Mg;④40K;⑤40Ca.
①18O;②12C;③26Mg;④40K;⑤40Ca.
| A、①② | B、②⑤ | C、只有④ | D、③④ |
下列各组粒子中质子数和电子数均相同的是( )
| A、CH4、H2O、Na+ |
| B、F2、Ar、HCl |
| C、H3O+、NH4+、Na |
| D、O2-、Mg2+、Ne |
下列有关氢化物的叙述中正确的是( )
| A、稳定性:HF>H2S>H2O |
| B、沸点:H2O>NH3>PH3 |
| C、一个D2O分子中所含的中子数为12 |
| D、在卤化氢中HF的还原性最强 |
下列说法正确的是( )
| A、碱性:LiOH>NaOH>KOH>RbOH |
| B、金属性:Rb>K>Na>Li |
| C、和酸反应时Fe失2个e-,Na失1个e-则Fe的金属性强于Na |
| D、Rb不易与水反应放出H2 |
重水( 21D2O)是重要的核工业原料,下列说法错误的是( )
| A、氘(D)原子核外有1个电子 |
| B、1H与D互称同位素 |
| C、H2O与D2O互称同素异形体 |
| D、1H218O与D216O的相对分子质量相同 |
 C:CH2=CH-CH=CH3-CH3 D:
C:CH2=CH-CH=CH3-CH3 D: E:
E: F:CH≡CH G:CH3-C≡CH H:CH3-C≡C-CH 3
F:CH≡CH G:CH3-C≡CH H:CH3-C≡C-CH 3 ,若要合成
,若要合成 ,则下列所选原料正确的是
,则下列所选原料正确的是