题目内容
有A、B、C、D四种元素,已知:A的最高价与其负价的代数和为6;A、D次外层电子都是8个,A和D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子;B是形成化合物种类最多的元素;C2-离子与氩原子具有相同的电子层结构.试写出:
(1)各元素的符号:A ,B ,C ,D .
(2)B的最高价氧化物的电子式为 ;用电子式表示D与C形成化合物的过程为 .
(3)A、D分别对应的最高价氧化物水化物之间反应的离子方程式 .
(1)各元素的符号:A
(2)B的最高价氧化物的电子式为
(3)A、D分别对应的最高价氧化物水化物之间反应的离子方程式
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:A、B、C、D四种元素,C2-离子与氩原子具有相同的电子层结构,则C为硫元素;B是形成化合物种类最多的元素,故B为碳元素;A的最高正价与其最低负价的代数和为6,则A处于ⅦA族,A次外层电子数是8个,则A为氯元素;D次外层电子数是8个,A和D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子,A离子带1个单位负电荷,核外电子数为18,所以D的阳离子带1个单位正电荷,核外电子数为18,故D为钾元素,据此解答.
解答:
解:A、B、C、D四种元素,C2-离子与氩原子具有相同的电子层结构,则C为硫元素;B是形成化合物种类最多的元素,故B为碳元素;A的最高正价与其最低负价的代数和为6,则A处于ⅦA族,A次外层电子数是8个,则A为氯元素;D次外层电子数是8个,A和D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子,A离子带1个单位负电荷,核外电子数为18,所以D的阳离子带1个单位正电荷,核外电子数为18,故D为钾元素,
(1)由上述分析可知,A为Cl、B为C、C为S、D为K,故答案为:Cl;C;S;K;
(2)B为C元素,最高价氧化物为CO2,分子中碳原子与氧原子之间形成2对共用电子对,其电子式为: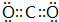 ,
,
D与C形成化合物为K2S,属于离子化合物,用K原子、S原子电子式表示其形成过程为: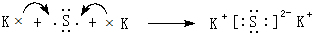 ,
,
故答案为: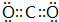 ;
;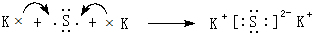 ;
;
(3)A、D分别对应的最高价氧化物水化物分别为HClO4、KOH,二者反应生成KClO4与水,反应离子方程式为:H++OH-═H2O,故答案为:H++OH-═H2O.
(1)由上述分析可知,A为Cl、B为C、C为S、D为K,故答案为:Cl;C;S;K;
(2)B为C元素,最高价氧化物为CO2,分子中碳原子与氧原子之间形成2对共用电子对,其电子式为:
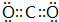 ,
,D与C形成化合物为K2S,属于离子化合物,用K原子、S原子电子式表示其形成过程为:
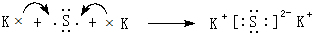 ,
,故答案为:
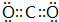 ;
;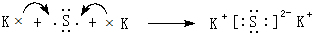 ;
;(3)A、D分别对应的最高价氧化物水化物分别为HClO4、KOH,二者反应生成KClO4与水,反应离子方程式为:H++OH-═H2O,故答案为:H++OH-═H2O.
点评:本题考查结构与位置关系、电子式等,难度不大,推断元素是关键,注意掌握用电子式表示化学键或物质的形成.

练习册系列答案
 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案
相关题目
下列电子式书写错误的是( )
A、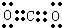 |
B、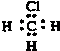 |
C、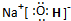 |
D、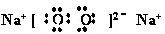 |
设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A、1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA |
| B、0.1mol丙烯酸中含有双键的数目为0.1NA |
| C、标准状况下,11.2L苯中含有分子的数目为0.5NA |
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4NA |
从碘水溶液中提取碘,可选用的分离方法为( )
| A、萃取分液法 | B、过滤法 |
| C、结晶法 | D、蒸馏法 |