��Ŀ����
��10�֣��������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����C02�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӡ�
(1)���й���C02����;����ȷ���� ������ţ���
A��������̼������ˮ������������̼��������
B�����������̼�׳Ƹɱ����������˹�����
C��������̼�����������Ϊ�����˿�ȼ����Ż��
D�����ٽ������̼����ȡ�ܼ����ڴ���Ȼ������ȡ�;����������
E��������̼������Ϊ���ʣ����ũ����IJ���
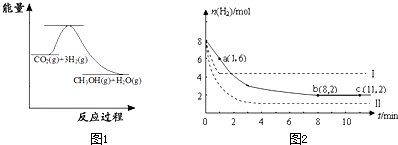
(2)Ŀǰ��ҵ����һ�ַ�������C02�������״���Ϊ̽���䷴Ӧԭ�����ֽ�������ʵ�飬�����Ϊ1L���ܱ������У�����1 mol CO2��3 mol H2��һ�������·�����Ӧ��C02(g)+
3 H2(g) 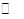 CH30H(g)+H20(g)
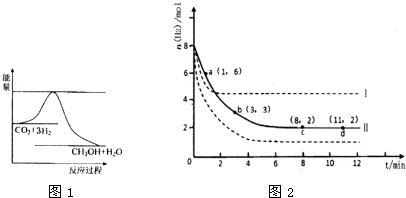
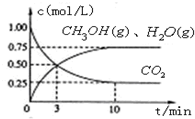
��H=-49.0kJ��m01-1�����C02��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��
CH30H(g)+H20(g)
��H=-49.0kJ��m01-1�����C02��CH3OH(g)��Ũ����ʱ��仯��ͼ��ʾ��

�ٴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ���ʣ�v(H��)= ��
�ڸ÷�Ӧ��ƽ�ⳣ��Ϊ ��
(3)��KHC03��ҺΪ����ʣ��õ��ķ���Ҳ���Խ�C02��ԭΪ�״�����д�����ʱ���������ӷ���ʽ��
(4)���ʯ��ʯīϩ������̼��̼�ļ���ͬ�������塣�Ӽ������ͷ������ǵ��ȶ�����ǿ������˳��Ϊ

��10�֣�
��1��C ��2�֣�
��2�� ��0.225mol•L-1•min-1��2�֣��� �� 5.33( mol•L-1)-2 ����λ����Ҫ��2�֣�
��3��CO2+6HCO3-+6e-=CH3OH+6CO32-+H2O����CO2+5H2O+6e-=CH3OH+6OH -����2�֣�
��4������̼>ʯīϩ>���ʯ��2�֣�
��������

 ��У����ϵ�д�
��У����ϵ�д�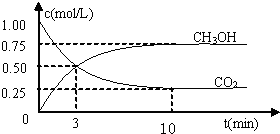 �������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ��ע
�������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ��ע