题目内容
把6.2g Na2O溶解于93.8g水中,得到的溶液的溶质质量分数为 .
考点:化学方程式的有关计算,溶液中溶质的质量分数及相关计算
专题:计算题
分析:发生反应:Na2O+H2O=2NaOH,根据方程式计算生成NaOH的质量,溶液质量=氧化钠质量+水的质量,进而计算氢氧化钠的质量分数.
解答:
解:设生成NaOH的质量为m,则:
Na2O+H2O=2NaOH
62 80
6.2g m
所以m=
=8g
溶液质量为6.2g+93.8g=100g
故所得溶液NaOH的质量分数为
×100%=8%,
故答案为:8%.
Na2O+H2O=2NaOH
62 80
6.2g m
所以m=
| 6.2g×80 |
| 62 |
溶液质量为6.2g+93.8g=100g
故所得溶液NaOH的质量分数为
| 8g |
| 100g |
故答案为:8%.
点评:本题考查化学方程式计算、质量分数计算,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案
相关题目
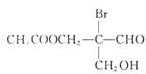 有机物若含手性碳原子(连接四个不同的原子或原子团的碳原子)就具有光学活性,如图物质发生下列反应后生成的有机物仍有光学活性的是( )
有机物若含手性碳原子(连接四个不同的原子或原子团的碳原子)就具有光学活性,如图物质发生下列反应后生成的有机物仍有光学活性的是( )①与甲酸、浓硫酸共热 ②与NaOH水溶液共热 ③与银氨溶液作用
④在Cu催化下与O2共热 ⑤在Ni催化下与氢气反应.
| A、仅③ | B、仅①③ |
| C、仅②④⑤ | D、①②③④⑤ |
下列叙述中,正确的是( )
| A、在AgBr饱和溶液中加入AgNO3溶液,达到平衡时,溶液中Br-浓度降低 |
| B、常温下,某溶液中由水电离出的c(OH-)=1×10-10mol/L,该溶液一定呈酸性 |
| C、FeCl3溶液和Fe2(SO4)3溶液加热蒸干,灼烧都得到Fe2O3 |
| D、向饱和碳酸钠溶液中通入足量二氧化碳,可以析出纯碱晶体 |

