题目内容
在pH=1的无色溶液中,可以大量共存的一组离子是( )
| A、Na+K+HCO3-Cl- |
| B、NH4+Mg2+SO42-Cl- |
| C、K+Na+ SO42- S2O32- |
| D、K+ Na+ AlO2- NO3- |
考点:离子共存问题
专题:离子反应专题
分析:无色溶液可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,pH=1的溶液中存在大量氢离子,
A.碳酸氢根离子与氢离子反应生成二氧化碳气体;
B.NH4+、Mg2+、SO42-、Cl-之间不发生反应,都不与氢离子反应,且为无色溶液;
C.S2O32-与氢离子反应生成二氧化硫气体和硫单质;
D.偏铝酸根离子与氢离子反应.
A.碳酸氢根离子与氢离子反应生成二氧化碳气体;
B.NH4+、Mg2+、SO42-、Cl-之间不发生反应,都不与氢离子反应,且为无色溶液;
C.S2O32-与氢离子反应生成二氧化硫气体和硫单质;
D.偏铝酸根离子与氢离子反应.
解答:
解:溶液无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,pH=1的溶液中存在大量氢离子,
A.HCO3-与氢离子反应生成二氧化碳气体,在溶液中不能大量共存,故A错误;
B.NH4+、Mg2+、SO42-、Cl-之间不反应,都不与氢离子反应,且为无色溶液,在溶液中能够大量共存,故B正确;
C.S2O32-与溶液中氢离子反应生成二氧化硫气体和硫单质,在溶液中不能大量共存,故C错误;
D.AlO2-离子与溶液中氢离子反应生成氢氧化铝沉淀或铝离子,在溶液中不能大量共存,故D错误;
故选B.
A.HCO3-与氢离子反应生成二氧化碳气体,在溶液中不能大量共存,故A错误;
B.NH4+、Mg2+、SO42-、Cl-之间不反应,都不与氢离子反应,且为无色溶液,在溶液中能够大量共存,故B正确;
C.S2O32-与溶液中氢离子反应生成二氧化硫气体和硫单质,在溶液中不能大量共存,故C错误;
D.AlO2-离子与溶液中氢离子反应生成氢氧化铝沉淀或铝离子,在溶液中不能大量共存,故D错误;
故选B.
点评:本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
下列物质与稀盐酸反应,能用离子方程式HCO3-+H+=CO2↑+H2O表示的是( )
| A、NaOH溶液 |
| B、Na2CO3溶液 |
| C、CaCO3 |
| D、NaHCO3溶液 |
以下实验不能获得成功的是( )
| A、将铜丝在酒精灯上加热后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
| B、除去溴苯中的少量Br2时加入KI溶液,充分反应后,弃去水溶液 |
| C、用适量苯和液溴混合制溴苯时,只需加铁屑,不必加热 |
| D、提取溶解在水中的少量碘时加入CCl4,分液,取出有机层再蒸馏 |
除去Na2CO3固体中少量NaHCO3的最佳方法是( )
| A、加入适量盐酸 |
| B、加入NaOH溶液 |
| C、加热 |
| D、配成溶液后通入CO2 |
下列说法正确的是( )
| A、用硫酸铁作净水剂 |
| B、自来水厂用盐酸进行消毒杀菌 |
| C、用苏打治疗胃酸过多 |
| D、用铝制餐具长时间存放咸的食物 |
解释下列过程的方程式正确的是( )
A、氯化钠溶于水发生电离,电离方程式为:NaCl
| ||||
| B、用过量氨水吸收烟道气中的SO2:SO2+2NH3?H2O═SO32-+2NH4++H2O | ||||
C、工业冶炼金属铝:AlCl3(熔融)
| ||||
| D、向物质的量之比为1:1的NaOH和Na2CO3混合物中加入过量稀盐酸:OH-+CO32-+2H+═HCO3-+H2O |
下列离子方程式书写正确的是( )
| A、NaHCO3溶液与NaOH溶液反应OH-+HCO3-=CO32-+H2O |
| B、铁和稀硫酸反应2Fe+6H+=2Fe3++3H2↑ |
| C、钠与CuSO4溶液反应:2Na+Cu2+=2Na++Cu |
| D、FeCl2溶液跟Cl2反应Fe2++Cl2=Fe3++2Cl- |
用光洁的铂丝蘸取某无色溶液,在无色火焰上灼烧时,观察到黄色火焰,则无色溶液中一定含有( )
| A、Cu2+ |
| B、K+ |
| C、Na+ |
| D、Ba2+ |
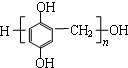 单体是
单体是 单体是
单体是