题目内容
7.观察下列实验装置图,按要求作答:
(1)装置中c、d、e的名称分别为蒸馏烧瓶、冷凝管、分液漏斗
(2)分离下列物质,需要在哪套装置中进行
Ⅰ.干燥H2,可采用⑤(填装置序号)装置
Ⅱ.除去食盐溶液中的水,可采用②(填装置序号)装置
Ⅲ.淡化食盐水,可采用③(填装置序号)装置
Ⅳ.实验室中的石灰水久置,液面上常悬浮有CaCO3微粒.可采用①(填装置序号)装置除去Ca(OH)2溶液中悬浮的CaCO3微粒
Ⅴ.分离碘水中的碘应先选择装置④(填装置序号) 进行萃取 和分液操作,再用装置③(填装置序号)进行蒸馏 操作.
分析 (1)由图可知仪器的名称;
(2)I.干燥气体利用洗气瓶;
Ⅱ.除去食盐溶液中的水,选择蒸发装置;
Ⅲ.淡化食盐水,选择蒸馏装置;
Ⅳ.实验室中的石灰水久置,液面上常悬浮有CaCO3微粒选择过滤状态;
Ⅴ.分离碘水中的碘,加萃取剂、萃取后,分液、蒸馏即可.
解答 解:(1)由图可知装置中c、d、e的名称分别为蒸馏烧瓶、冷凝管、分液漏斗,故答案为:蒸馏烧瓶;冷凝管;分液漏斗;
(2)Ⅰ.干燥H2,可采用⑤装置,导管长进短出,故答案为:⑤;
Ⅱ.除去食盐溶液中的水,可采用②装置,故答案为:②;
Ⅲ.淡化食盐水,可采用③装置,故答案为:③;
Ⅳ.实验室中的石灰水久置,液面上常悬浮有CaCO3微粒.可采用①装置除去Ca(OH)2溶液中悬浮的CaCO3微粒,故答案为:①;
Ⅴ.分离碘水中的碘应先选择装置④进行萃取和分液操作,再用装置③进行蒸馏操作,故答案为:④;萃取;分液;③;蒸馏.
点评 本题考查混合物分离提纯,为高频考点,把握仪器的使用、混合物分离提纯实验装置及应用为解答的关键,侧重分析与实验能力的考查,综合性较强,题目难度不大.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案 教育世家状元卷系列答案
教育世家状元卷系列答案 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
17.“绿色化学”对化学反应提出了“原子经济性”(原子节约)的新概念及要求,理想原子经济性反应是原料分子中的原子全部转化成所需要的产物,不产生副产物,实现零排放.下列反应类型一定符合这一要求的是( )
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤酯化反应 ⑥加聚反应.
①取代反应 ②加成反应 ③消去反应 ④水解反应 ⑤酯化反应 ⑥加聚反应.
| A. | ②④ | B. | ①④ | C. | ③⑤ | D. | ②⑥ |
18.在同温同压下,下列各组热化学方程式中,△H2>△H1的是( )
| A. | 2H2(g)+O2(g)=2H2O(g);△H12H2(g)+O2(g)=2H2O(l);△H2 | |
| B. | S(g)+O2(g)=SO2(g);△H1S(s)+O2(g)=SO2(g);△H2 | |
| C. | CO(g)+$\frac{1}{2}$O2(g)=CO2(g);△H12CO(g)+O2(g)=2CO2(g);△H2 | |
| D. | H2(g)+Cl2(g)=2HCl(g);△H1$\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)=HCl(g);△H2 |
2.用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 含有NA个氮原子的氮气在标准状况下的体积约为11.2L | |
| B. | 25℃,1.01×105Pa,64g SO2中含有的原子数小于3NA | |
| C. | 在常温常压下,11.2LCl2含有的分子数为0.5NA | |
| D. | 标准状况下,11.2L H2O含有的分子数为0.5NA |
12.2H2(g)+O2(g)═2H2O(l);△H=-571.6kJ•mol-1、CO(g)+O2(g)=CO2(g)△H=-283kJ•mol-1某H2和CO的混合气体完全燃烧时放出113.74kJ热量,同时生成3.6g液态水,则原混合气体的H2和CO的物质的量之比( )
| A. | 2:1 | B. | 1:2 | C. | 1:1 | D. | 2:3 |
19.食品中可以按规定加入一定量的食品添加剂、干燥剂或除氧剂,下列说法正确的是( )
| A. | 补血营养品红桃K中添加微量铁粉,作为补铁剂 | |
| B. | 中秋月饼包装袋内有小袋铁粉,作为干燥剂 | |
| C. | 苏打饼干包装盒中有小袋生石灰,作为补钙剂 | |
| D. | 卤制品中加入大量亚硝酸钠,作为保鲜剂 |
16.把0.05molNaOH固体分别加入到100ml下列液体中,溶液导电能力变化最小的是( )
| A. | 自来水 | B. | 0.5mol/L盐酸 | C. | 0.5mol/LHAc溶液 | D. | 0.5mol/LKCl溶液 |
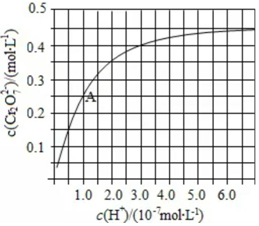 元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4-(绿色)、Cr2O72-(橙红色)、CrO42-(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题: