题目内容
10.实验室需配制一种仅含五种离子(水电离出的离子可忽略)的混合溶液,且在混合溶液中五种离子的物质的量浓度均为1mol/L.,下面四个选项中能达到此目的是( )| A. | Al3+、K+、SO42-、Cl-、Al[(OH)4]- | B. | Al3+、Na+、Cl-、SO42-、NO3- | ||
| C. | Na+、K+、SO42-、NO3-、Cl- | D. | Fe2+、H+、Br-、NO3-、Cl- |
分析 混合溶液中五种离子的物质的量浓度均为1mol•L-1,应满足溶液呈电中性的特点,如离子之间不发生复分解、氧化还原反应以及互促水解反应,则可大量共存,以此判断.
解答 解:A.Al3+与Al[(OH)4]-发生互促水解而不能大量共存,故A错误;
B.符合电荷守恒,且离子之间不发生任何反应,能大量共存,故B正确;
C.各离子浓度相等时,溶液中总电荷不守恒,故C错误;
D.符合电荷守恒,但Fe2+和NO3-在酸性条件下不能大量共存,故D错误;
故选B.
点评 本题考查离子共存问题,题目难度不大,侧重于元素化合物知识的综合应用,为高考常见题型,注意把握相关离子的性质,易错点为C,注意溶液电荷守恒的应用.

练习册系列答案
相关题目
20.在一个恒容绝热的密闭容器中,发生可逆反应:M(?)+2N(g)?P(g)+Q(g) 该反应为吸热反应,已知M的状态未知,则下列描述一定达到平衡的标志是( )
①当物质M、N、P的体积分数比为 1:1:1时 ②混合气体的密度不变时
③体系的温度不变时 ④反应速率2v (N)正=v (Q)逆时
⑤体系的压强不变时 ⑥气体的平均相对分子质量不变时.
①当物质M、N、P的体积分数比为 1:1:1时 ②混合气体的密度不变时
③体系的温度不变时 ④反应速率2v (N)正=v (Q)逆时
⑤体系的压强不变时 ⑥气体的平均相对分子质量不变时.
| A. | ①③④ | B. | ③⑤⑥ | C. | ②③⑥ | D. | ③④⑤ |
1.乙醇分子结构中各化学键如图所示.关于乙醇在各种反应中断键说法不正确的是( )
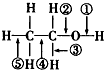
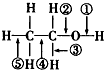
| A. | 在银催化条件下与O2反应时断裂①和③ | |
| B. | 乙醇燃烧是断裂②和⑤ | |
| C. | 和金属钠反应时①断裂 | |
| D. | 和浓H2SO4、乙酸共热时断裂①,其他键不变化 |
18.铜、铬都是用途广泛的金属.工业上利用电镀污泥(主要含有Fe2O3、CuO、Cr2O3及部分难溶杂质)回收金属铜和铬的流程如图1:
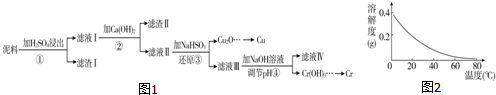
已知:部分物质沉淀的pH如表:
CaSO4的溶解度曲线如图2.
请回答下列问题:
(1)滤液Ⅰ中所含溶质主要有Fe2(SO4)3、Cr2(SO4)3、CuSO4(填化学式).
(2)第②步操作中,先加入Ca(OH)2调节溶液的pH,调节范围为3.2≤pH<4.3,然后将浊液加热至80℃趁热过滤,所得滤渣Ⅱ的成分为Fe(OH)3、CaSO4.
(3)第③步操作中,发现除了生成砖红色沉淀外,还产生了无色刺激性气味的气体.写出该步骤中发生反应的离子方程式2H2O+HSO3-+2Cu2+=Cu2O↓+SO42-+5H+、HSO3-+H+=SO2↑+H2O.
(4)当离子浓度≤1×10-5 mol•L-1时,可以认为离子沉淀完全.第④步操作中,若要使Cr3+完全沉淀,则室温下溶液中a的最小值为5.6.已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{64}$≈4.0;lg 4=0.6.
(5)Cr(OH)3受热分解为Cr2O3,用铝热法可以冶炼金属铬.写出铝热法炼铬的化学方程式Cr2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Cr.

已知:部分物质沉淀的pH如表:
| Fe3+ | Cu2+ | Cr3+ | |
| 开始沉淀pH | 2.1 | 4.7 | 4.3 |
| 完全沉淀pH | 3.2 | 6.7 | a |
请回答下列问题:
(1)滤液Ⅰ中所含溶质主要有Fe2(SO4)3、Cr2(SO4)3、CuSO4(填化学式).
(2)第②步操作中,先加入Ca(OH)2调节溶液的pH,调节范围为3.2≤pH<4.3,然后将浊液加热至80℃趁热过滤,所得滤渣Ⅱ的成分为Fe(OH)3、CaSO4.
(3)第③步操作中,发现除了生成砖红色沉淀外,还产生了无色刺激性气味的气体.写出该步骤中发生反应的离子方程式2H2O+HSO3-+2Cu2+=Cu2O↓+SO42-+5H+、HSO3-+H+=SO2↑+H2O.
(4)当离子浓度≤1×10-5 mol•L-1时,可以认为离子沉淀完全.第④步操作中,若要使Cr3+完全沉淀,则室温下溶液中a的最小值为5.6.已知:Ksp[Cr(OH)3]=6.3×10-31,$\root{3}{64}$≈4.0;lg 4=0.6.
(5)Cr(OH)3受热分解为Cr2O3,用铝热法可以冶炼金属铬.写出铝热法炼铬的化学方程式Cr2O3+2Al$\frac{\underline{\;高温\;}}{\;}$Al2O3+2Cr.
5.下列说法不正确的是( )
| A. | 用洁净铂丝蘸取未知溶液进行焰色反应,呈黄色火焰,则该溶液有Na+,但不能确定K+的存在 | |
| B. | 实验室制取乙酸乙酯时,向试管中加入乙醇,然后边摇动试管边慢慢加入浓硫酸和冰醋酸 | |
| C. | 用已知浓度NaOH溶液滴定未知浓度盐酸,滴定终点时,俯视刻度线,则测得盐酸浓度偏小 | |
| D. | 相同温度下,可以通过观察气泡多少来比较不同浓度Na2SO3溶液与稀H2SO4溶液反应的快慢 |
15.苯环结构中不存在C-C与C═C的简单交替排列结构,可以作为证据的事实是( )
①苯不能使酸性KMnO4溶液褪色
②苯不能使溴水因化学反应而褪色
③经实验测定只有一种结构的邻二甲苯
④苯能在加热和催化剂条件下氢化成环己烷
⑤苯中相邻C原子与C原子间的距离都相等.
①苯不能使酸性KMnO4溶液褪色
②苯不能使溴水因化学反应而褪色
③经实验测定只有一种结构的邻二甲苯
④苯能在加热和催化剂条件下氢化成环己烷
⑤苯中相邻C原子与C原子间的距离都相等.
| A. | 只有①②③⑤ | B. | 只有④⑤ | C. | ①②③④⑤ | D. | 只有①② |
2.透明强酸性溶液中,下列各组离子一定能大量共存的是( )
| A. | Cl-、Cu2+、SO42-、NO3- | B. | Cl-、Na+、SO42-、CH3COO- | ||
| C. | Cl-、Fe2+、MnO4-、NO3- | D. | AlO2-、Na+、SO42-、NO3- |
13.A、B、C、D、E五种短周期主族元素原子序数逐渐增大,其中A与C、B与E分别为同族元素.原子半径A<B<E<D<C,B原子最外层电子数是次外层的3倍,C、D的核外电子数之和与B、E核外电子数之和相等.下列说法正确的是( )
| A. | 简单离子半径:E<D | |
| B. | 气态氢化物的稳定性:B<E | |
| C. | 最高价氧化物对应水化物的碱性:C>D | |
| D. | A与E形成的化合物为离子化合物 |