题目内容
醛与银氨溶液的反应常因条件控制不当会出现各种现象而影响银镜反应的效果.
某研究小组为探究乙醛发生银镜反应的最佳实验条件,进行了有关实验,相关数据如下表:
请回答下列问题:
(1)下列有关制备银镜的实验过程的说法中正确的是(选填下列选项字母)
A.先将试管加碱液煮沸,然后再用蒸馏水洗净
B.向洁净试管中加入1mL 2%的AgNO3溶液,边滴入2%的稀氨水边振荡,直到产生的沉淀又刚好溶解为止
C.将几滴银氨溶液滴人2mL乙醛溶液试管中
D.将试管放在沸水浴中加热即可产生光亮银镜
E.银氨溶液具有较强的氧化性和碱性
(2)“加热”在化学实验实验中较为常见,下列仪器中能用酒精灯直接加热的有 (填字母)
①集气瓶②试管③量筒④烧杯⑤表面皿⑥蒸发皿⑦容量瓶⑧锥形瓶⑨干燥管⑩坩埚
A ①②③⑤⑥B ②③④⑦⑧C ②⑥⑩D ②⑤⑥⑨⑩
(3)写出乙醛与银氨溶液反应的离子方程式 .
(4)若只进行实验1和实验2,其探究的目的是 .
(5)实验 (填序号)组合,可探究混合液的PH对银镜反应的影响.
(6)实验4无银镜出现的原因是 .
(7)试管内壁的银镜可用硝酸洗涤以回收硝酸银溶液,你认为选用 (填“浓硝酸”或“稀硝酸”)较好,理由是 .
某研究小组为探究乙醛发生银镜反应的最佳实验条件,进行了有关实验,相关数据如下表:
| 实验变量实验序号 | 银氨溶液 的量/ml | 乙醛的量 /滴 | 水浴温度 /℃ | 反应混合 液的PH | 出现银镜的 时间/min |
| 1 | 2 | 3 | 50 | 11 | T1 |
| 2 | 2 | 3 | 65 | 11 | T2 |
| 3 | 2 | 5 | 65 | 11 | T3 |
| 4 | 2 | 5 | 65 | 4 | 无银镜 |
| 5 | 2 | 5 | 65 | 10 | T4 |
| 6 | 4 | 3 | 50 | 10 | T5 |
(1)下列有关制备银镜的实验过程的说法中正确的是(选填下列选项字母)
A.先将试管加碱液煮沸,然后再用蒸馏水洗净
B.向洁净试管中加入1mL 2%的AgNO3溶液,边滴入2%的稀氨水边振荡,直到产生的沉淀又刚好溶解为止
C.将几滴银氨溶液滴人2mL乙醛溶液试管中
D.将试管放在沸水浴中加热即可产生光亮银镜
E.银氨溶液具有较强的氧化性和碱性
(2)“加热”在化学实验实验中较为常见,下列仪器中能用酒精灯直接加热的有
①集气瓶②试管③量筒④烧杯⑤表面皿⑥蒸发皿⑦容量瓶⑧锥形瓶⑨干燥管⑩坩埚
A ①②③⑤⑥B ②③④⑦⑧C ②⑥⑩D ②⑤⑥⑨⑩
(3)写出乙醛与银氨溶液反应的离子方程式
(4)若只进行实验1和实验2,其探究的目的是
(5)实验
(6)实验4无银镜出现的原因是
(7)试管内壁的银镜可用硝酸洗涤以回收硝酸银溶液,你认为选用
考点:性质实验方案的设计
专题:实验设计题
分析:(1)A.将试管加碱液煮沸,促进油脂水解;
B.制备银氨溶液时将氨水滴入硝酸银溶液中,而不是将硝酸银滴入银氨溶液中;
C.银镜反应必须是在碱性条件下进行;
D.有机反应较缓慢;
E.银氨溶液具有弱氧化性和碱性;
(2)能用酒精灯直接加热的仪器有:试管、蒸发皿、坩埚;
(3)乙醛和银氨溶液发生氧化还原反应生成乙酸铵、氨气、Ag和水;
(4)实验1和实验2的不同点是温度,所以其目的是研究温度对反应的影响;
(5)探究混合液的PH对银镜反应的影响,应该只有pH不同,其它条件都相同;
(6)酸性条件下不发生银镜反应;
(7)浓稀硝酸都可以和Ag反应除去Ag,N元素化合价变化大的需要的硝酸少.
B.制备银氨溶液时将氨水滴入硝酸银溶液中,而不是将硝酸银滴入银氨溶液中;
C.银镜反应必须是在碱性条件下进行;
D.有机反应较缓慢;
E.银氨溶液具有弱氧化性和碱性;
(2)能用酒精灯直接加热的仪器有:试管、蒸发皿、坩埚;
(3)乙醛和银氨溶液发生氧化还原反应生成乙酸铵、氨气、Ag和水;
(4)实验1和实验2的不同点是温度,所以其目的是研究温度对反应的影响;
(5)探究混合液的PH对银镜反应的影响,应该只有pH不同,其它条件都相同;
(6)酸性条件下不发生银镜反应;
(7)浓稀硝酸都可以和Ag反应除去Ag,N元素化合价变化大的需要的硝酸少.
解答:
解:(1)A.将试管加碱液煮沸,促进油脂水解,防止影响银镜反应,故正确;
B.制备银氨溶液时将氨水滴入硝酸银溶液中,而不是将硝酸银滴入银氨溶液中,其制备方法为向洁净试管中加入1mL 2%的AgNO3溶液,边滴入2%的稀氨水边振荡,直到产生的沉淀又刚好溶解为止,故正确;
C.银镜反应必须是在碱性条件下进行,所以将几滴银氨溶液滴人2mL乙醛溶液试管中不能确定溶液呈碱性,故错误;
D.有机反应较缓慢,所以将试管放在沸水浴中加热不能立即产生光亮银镜,故错误;
E.银氨溶液中氨水过量,溶液呈碱性,且具有弱氧化性,故错误;
故选AB;
(2)能用酒精灯直接加热的仪器有:试管、蒸发皿、坩埚,不能加热的仪器有:集气瓶、量筒、表面皿、容量瓶、干燥管,需要垫石棉网加热的仪器有:烧杯、锥形瓶,
故选C;
(3)乙醛和银氨溶液发生氧化还原反应生成乙酸铵、氨气、Ag和水,反应方程式为CH3CHO+2Ag(NH3)2++2OH -
CH3COO-+NH4++3NH3+2Ag↓+H2O,
故答案为:CH3CHO+2Ag(NH3)2++2OH-
CH3COO-+NH4++3NH3+2Ag↓+H2O;
(4)实验1和实验2的不同点是温度,所以其目的是研究温度对反应的影响,
故答案为:研究温度对银镜反应的影响;
(5)探究混合液的PH对银镜反应的影响,应该只有pH不同,其它条件都相同,所以3、4、5能实现目的,故答案为:3、4、5;
(6)pH=4时,该反应呈酸性,酸性条件下没有产生银镜反应,pH>7时溶液呈碱性,碱性条件下能发生银镜反应,所以银镜反应必须在碱性条件下才能实现,
故答案为:银镜反应需要在碱性条件下进行;
(7)浓稀硝酸都可以和Ag反应除去Ag,
3Ag+4HNO3=3AgNO3+NO↑+2H2O、Ag+2HNO3(浓)=AgNO3+NO2↑+H2O,根据方程式知,溶解相同物质的量的Ag,浓硝酸消耗的多,所以稀硝酸的利用率高,所以选稀硝酸,
故答案为:稀硝酸;稀硝酸的利用率高(或产生等物质的量的硝酸银时产生的有害气体少).
B.制备银氨溶液时将氨水滴入硝酸银溶液中,而不是将硝酸银滴入银氨溶液中,其制备方法为向洁净试管中加入1mL 2%的AgNO3溶液,边滴入2%的稀氨水边振荡,直到产生的沉淀又刚好溶解为止,故正确;
C.银镜反应必须是在碱性条件下进行,所以将几滴银氨溶液滴人2mL乙醛溶液试管中不能确定溶液呈碱性,故错误;
D.有机反应较缓慢,所以将试管放在沸水浴中加热不能立即产生光亮银镜,故错误;
E.银氨溶液中氨水过量,溶液呈碱性,且具有弱氧化性,故错误;
故选AB;
(2)能用酒精灯直接加热的仪器有:试管、蒸发皿、坩埚,不能加热的仪器有:集气瓶、量筒、表面皿、容量瓶、干燥管,需要垫石棉网加热的仪器有:烧杯、锥形瓶,
故选C;
(3)乙醛和银氨溶液发生氧化还原反应生成乙酸铵、氨气、Ag和水,反应方程式为CH3CHO+2Ag(NH3)2++2OH -
| △ |
故答案为:CH3CHO+2Ag(NH3)2++2OH-
| △ |
(4)实验1和实验2的不同点是温度,所以其目的是研究温度对反应的影响,
故答案为:研究温度对银镜反应的影响;
(5)探究混合液的PH对银镜反应的影响,应该只有pH不同,其它条件都相同,所以3、4、5能实现目的,故答案为:3、4、5;
(6)pH=4时,该反应呈酸性,酸性条件下没有产生银镜反应,pH>7时溶液呈碱性,碱性条件下能发生银镜反应,所以银镜反应必须在碱性条件下才能实现,
故答案为:银镜反应需要在碱性条件下进行;
(7)浓稀硝酸都可以和Ag反应除去Ag,
3Ag+4HNO3=3AgNO3+NO↑+2H2O、Ag+2HNO3(浓)=AgNO3+NO2↑+H2O,根据方程式知,溶解相同物质的量的Ag,浓硝酸消耗的多,所以稀硝酸的利用率高,所以选稀硝酸,
故答案为:稀硝酸;稀硝酸的利用率高(或产生等物质的量的硝酸银时产生的有害气体少).
点评:本题考查探究物质性质的实验,侧重考查学生分析问题、总结归纳能力,明确实验原理是解本题关键,会根据图表数据不同点进行分析,知道银氨溶液制备方法,题目难度不大.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目
在强碱性溶液中能大量共存,且溶液为无色透明的离子组是( )
| A、K+、MnO4-、Cl-、Ba2+ |
| B、Na+、Ba2+、HCO3-、NO3- |
| C、K+、NO3-、CO32-、Cl- |
| D、Na+、H+、Cl-、S2- |
粗盐中含有不溶性的泥沙和可溶性的Ca2+、Mg2+、SO42-等杂质,除去SO42-用加入什么试剂( )
| A、稀HCl |
| B、BaCl2 溶液 |
| C、AgNO3溶液 |
| D、稀HNO3 |
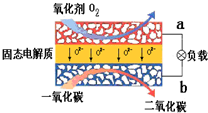 (1)有A、B、C、D四种金属,已知:只有D投入水中可与水剧烈反应;用B和C作电极,稀硫酸作电解质溶液构成原电池时,C为正极;A和C的离子共存于电解液中,以石墨为电极电解时阴极析出A.则这四种金属的活动性由强到弱的顺序是
(1)有A、B、C、D四种金属,已知:只有D投入水中可与水剧烈反应;用B和C作电极,稀硫酸作电解质溶液构成原电池时,C为正极;A和C的离子共存于电解液中,以石墨为电极电解时阴极析出A.则这四种金属的活动性由强到弱的顺序是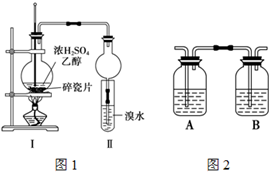 某化学兴趣小组用如图1所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色.
某化学兴趣小组用如图1所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性.当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓H2SO4与乙醇的混合液体变为棕黑色.