题目内容
14.下列说法错误的是( )| A. | 溶液是比胶体更稳定的分散系 | |
| B. | 相同状況下,1L空气与1LO2所含的分子数相等 | |
| C. | 相同状况下,1 L空气与1 L薄雾所含的分子数相等 | |
| D. | 20mL0.2 mol•L-1NaCl 溶液和 50mL0.1 mol•L-1 MgCl2 溶液中的 c((Cl- )相等 |
分析 A.分散质离子直径越小越稳定;
B.物质的量相同时含有分子数相同;
C.物质的量相同时含有分子数相同;
D.根据同一化学式中各微粒的浓度等于物质的物质的量浓度×离子个数,与溶液的体积无关.
解答 解:A.分散质离子直径越小越稳定,所以溶液是比胶体更稳定的分散系,故A正确;
B.根据N=nNA可知,相同状況下,1L空气与1LO2所含分子数相等,故B正确;
C.薄雾为液态,所以相同状况下,1 L空气与1 L薄雾物质的量不同,则所含的分子数不等,故C错误;
D.20mL0.2 mol•L-1NaCl 溶液中的Cl-的物质的量浓度c(Cl-)=0.2mol•L-1,50mL0.1mol•L-1 MgCl2溶液中的Cl-的物质的量浓度c(Cl-)=2c(MgCl2)=0.2mol•L-1,故D正确.
故选C.
点评 本题考查了分散系的稳定性、物质的量的计算,浓度的比较等,题目难度不大,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
4.常温下在下列溶液中加入足量的铁,充分反应后,生成气体最多的是( )
| A. | 20mL 12mol•L-1的盐酸 | B. | 10mL 18mol•L-1的硫酸 | ||
| C. | 80mL 2mol•L-1的硫酸 | D. | 40mL 14mol•L-1的硝酸 |
5.在给定条件下,下列选项所示的物质间转化均能实现的是( )
| A. | MgCO3$\stackrel{HCl(aq)}{→}$MgCl2(aq)$\stackrel{电解}{→}$Mg | |
| B. | NaCl(aq)$\stackrel{CO_{2}}{→}$NaHCO3$\stackrel{△}{→}$Na2CO3 | |
| C. | Cu2(OH)2CO3$\stackrel{△}{→}$CuO$\stackrel{H_{2}O}{→}$Cu(OH)2 | |
| D. | SO2$\stackrel{氨水}{→}$NH4HSO3$\stackrel{H_{2}SO_{4}(aq)}{→}$(NH4)2SO4 |
2.药物阿司匹林可由水杨酸制得,它们的结构如图所示.有关说法正确的是( )


| A. | 服用阿司匹林,身体出现水杨酸不良反应时,可静脉注射NaHCO3溶液 | |
| B. | 阿司匹林的分子式为C9H10O4 | |
| C. | 水杨酸可以发生取代、加成、氧化、加聚反应 | |
| D. | 1 mol阿司匹林最多可消耗2 mol NaOH |
9.在探究SO2水溶液成分和性质的实验中,下列根据实验现象得出的结论正确的是( )
| A. | 向SO2水溶液中加入少量NaHCO3粉末,有气泡产生,说明H2SO3酸性强于H2CO3 | |
| B. | 向SO2水溶液中滴加Ba(NO3)2溶液,有白色沉淀产生,说明SO2水溶液中含有SO42- | |
| C. | 向SO2水溶液中通入H2S气体,有淡黄色沉淀产生,说明SO2水溶液具有氧化性 | |
| D. | 向KMnO4溶液中滴加SO2水溶液,溶液颜色褪去,说明SO2水溶液具有漂白性 |
19.下列实验操作、实验现象和实验结论均正确的是( )
| A. | 在含有Fe3+的NaCl溶液中加入适量NaOH溶液,过滤,可除去杂质 | |
| B. | 将含有杂质HC1的Cl2通入饱和食盐水中,可收集到纯净的Cl2 | |
| C. | 某粉末中滴加盐酸,产生能使澄清石灰水变浑池的无色无味气体该粉末为碳酸盐 | |
| D. | 向某溶液中滴加酸化的Ba(NO3)2溶液,出现白色沉淀,则该溶液中含有SO42- |
6.我国古代文献资料中记载了大量的化学研究过程与成果.下列选项不涉及化学变化的是( )
| 选项 | A | B | C | D |
| 原文 | 欲去杂还纯,再入水煎炼,倾入盆中,经宿成白雪 | 以曾青凃铁,铁赤色如铜 | 丹砂烧之成水银,积变又还成丹砂 | 水火既济而土和 |
| 解释 | 重结晶方法提纯物质 | 金属的置换 | 物质间转化的可逆性 | 黏土烧结成陶瓷 |
| A. | A | B. | B | C. | C | D. | D |
3.在体积为2L的恒容密闭容器中发生反应xA(g)+yB(g)?zC(g),图1表示200℃时容器中A、B、C物质的量随时间的变化关系,图2表示不同温度下平衡时C的体积分数随起始n(A):n(B)的变化关系.则下列结论正确的是( )


| A. | 200℃时,反应从开始到平衡的平均速率v(B)=0.04mol•L-1•min-1 | |
| B. | 图2所知反应xA(g)+yB(g)?zC(g)的△H>0,且a=1 | |
| C. | 若在图1所示的平衡状态下,再向体系中充入He,此时v正>v逆 | |
| D. | 200℃时,向容器中充入2mol A和1mol B,达到平衡时,A的体积分数小于0.5 |
6.下列叙述正确的是( )

| A. | 将一小块铜片放入盛有浓硫酸的试管中加热反应后的溶液呈蓝色 | |
| B. | 将一小块钠放入盛有水的烧杯中,钠在水面上游动,同时看到烧杯内的溶液变为红色 | |
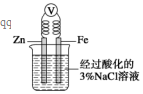
| C. | 如图,一段时间后给烧杯内的溶液中加入氢氧化钠溶液,可看到Fe电极附近有红褐色沉淀生成 | |
| D. | 向盛有少量Mg(OH)2沉淀悬浊液的试管中滴加氯化铵溶液,可看到沉淀溶解 |