题目内容
工业生产无铁硫酸铝,以硫酸浸取铝土矿得含铁(Fe2+和Fe3+)的硫酸铝溶液,加热到一定温度,搅拌,加入一定量高锰酸钾溶液和硫酸锰溶液,在溶液中生成活性二氧化锰,调节溶液的pH,反应一段时间,Fe(OH)3和二氧化锰发生吸附共沉作用,最终得到无铁硫酸铝产品.
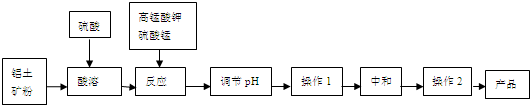
(1)KMnO4首先将Fe2+氧化为Fe3+,其本身被还原为MnO2,反应的离子方程式为 .
(2)写出高锰酸钾溶液和硫酸锰溶液反应的化学方程式 .实验证明,
控制在4:1时,除铁效果较好.若溶液中亚铁离子和铁离子浓度均为0.03mol/L,为达到较好的除铁效果,每1L溶液应加入高锰酸钾的物质的量为 .
(3)调节pH的作用是 .
(4)操作2的名称为 .
(5)下列有关工艺的说法正确的是 .(填字母序号)
A.溶液的pH越大,则除铁效果越好,但同时会影响硫酸铝的产率
B.活性二氧化锰生成量应适宜,不足时铁的去除率较低,过量时会增加成本
C.可以直接向溶液中加入二氧化锰粉末以除去Fe(OH)3.

(1)KMnO4首先将Fe2+氧化为Fe3+,其本身被还原为MnO2,反应的离子方程式为
(2)写出高锰酸钾溶液和硫酸锰溶液反应的化学方程式
| n(MnO2) |
| n(Fe) |
(3)调节pH的作用是
(4)操作2的名称为
(5)下列有关工艺的说法正确的是
A.溶液的pH越大,则除铁效果越好,但同时会影响硫酸铝的产率
B.活性二氧化锰生成量应适宜,不足时铁的去除率较低,过量时会增加成本
C.可以直接向溶液中加入二氧化锰粉末以除去Fe(OH)3.
考点:物质分离和提纯的方法和基本操作综合应用,制备实验方案的设计
专题:实验设计题
分析:工业生产无铁硫酸铝,以硫酸浸取铝土矿得含铁(Fe2+和Fe3+)的硫酸铝溶液,加热到一定温度,搅拌,加入一定量高锰酸钾溶液和硫酸锰溶液,在溶液中生成活性二氧化锰,调节溶液的pH,反应一段时间,Fe(OH)3和二氧化锰发生吸附共沉作用,最终得到无铁硫酸铝产品;
(1)KMnO4首先将Fe2+氧化为Fe3+,其本身被还原为MnO2,依据原子守恒和电荷守恒书写离子方程式;
(2)根据氧化还原反应中化合价升降相等,可写出化学方程式为2KMnO4+3MnSO4+2H2O=5MnO2↓+K2SO4+2H2SO4;结合离子方程式和化学方程式定量关系计算;
(3)铁离子易发生水解反应生成氢氧化铁;
(4)操作1为过滤,操作2为蒸发结晶;
(5)A.氢氧化钠与硫酸铝反应生成氢氧化铝沉淀;
B.活性二氧化锰不足时铁的去除率较低;
C.直接向溶液中加入二氧化锰粉末吸附作用太低;
(1)KMnO4首先将Fe2+氧化为Fe3+,其本身被还原为MnO2,依据原子守恒和电荷守恒书写离子方程式;
(2)根据氧化还原反应中化合价升降相等,可写出化学方程式为2KMnO4+3MnSO4+2H2O=5MnO2↓+K2SO4+2H2SO4;结合离子方程式和化学方程式定量关系计算;
(3)铁离子易发生水解反应生成氢氧化铁;
(4)操作1为过滤,操作2为蒸发结晶;
(5)A.氢氧化钠与硫酸铝反应生成氢氧化铝沉淀;
B.活性二氧化锰不足时铁的去除率较低;
C.直接向溶液中加入二氧化锰粉末吸附作用太低;
解答:
解:(1)KMnO4首先将Fe2+氧化为Fe3+,其本身被还原为MnO2,依据原子守恒和电荷守恒书写离子方程式为:MnO4-+3Fe2++4H+=3Fe3++MnO2+2H2O,
故答案为:MnO4-+3Fe2++4H+=3Fe3++MnO2+2H2O;
(2)由题意可知高锰酸钾溶液和硫酸锰溶液反应生成活性二氧化锰,根据氧化还原反应中化合价升降相等,可写出化学方程式为2KMnO4+3MnSO4+2H2O=5MnO2↓+K2SO4+2H2SO4,若溶液中亚铁离子和铁离子浓度均为0.03mol/L,溶液中含有Fe2+物质的量为0.03mol,调节溶液PH使铁离子全部沉淀,n(Fe)=0.06mol
MnO4-+3Fe2++4H+=3Fe3++MnO2+2H2O,
0.01mol 0.03mol 0.01mol
控制在4:1时,除铁效果较好.则n(MnO2)=0.06mol×4=0.24mol;
反应中生成二氧化锰物质的量=0.24mol-0.01mol=0.23mol,消耗高锰酸钾物质的量:
2KMnO4+3MnSO4+2H2O=5MnO2↓+K2SO4+2H2SO4,
2 5
n 0.23mol
n=0.0.092mol
为达到较好的除铁效果,每1L溶液应加入高锰酸钾的物质的量=0.092mol+0.01mol=0102mol;
故答案为:2KMnO4+3MnSO4+2H2O=5MnO2↓+K2SO4+2H2SO4;0.102mol;
(3)铁离子易发生水解反应生成氢氧化铁,当调节溶液PH,使溶液PH增大时,易使铁离子转化为氢氧化铁沉淀除去,
故答案为:使铁离子转化为氢氧化铁沉淀除去;
(4)根据题中信息,反应一段时间,二氧化锰和Fe (OH) 3发生吸附共沉作用,可知操作1为过滤,操作2为过滤后,滤液蒸发浓缩,冷却结晶,过滤洗涤;
故答案为:过滤,蒸发浓缩,冷却结晶,过滤洗涤;
(5)A.如果溶液的碱性太强,会与硫酸铝反应生成氢氧化铝沉淀而导致产率较低,故A错误;
B.活性二氧化锰不足时不能完全除去氢氧化铁,铁的去除率较低,过量时会增加成本,故B正确;
C.直接向溶液中加入二氧化锰粉末吸附作用太低,故C错误.
故答案为:B.
故答案为:MnO4-+3Fe2++4H+=3Fe3++MnO2+2H2O;
(2)由题意可知高锰酸钾溶液和硫酸锰溶液反应生成活性二氧化锰,根据氧化还原反应中化合价升降相等,可写出化学方程式为2KMnO4+3MnSO4+2H2O=5MnO2↓+K2SO4+2H2SO4,若溶液中亚铁离子和铁离子浓度均为0.03mol/L,溶液中含有Fe2+物质的量为0.03mol,调节溶液PH使铁离子全部沉淀,n(Fe)=0.06mol
MnO4-+3Fe2++4H+=3Fe3++MnO2+2H2O,
0.01mol 0.03mol 0.01mol
| n(MnO2) |
| n(Fe) |
反应中生成二氧化锰物质的量=0.24mol-0.01mol=0.23mol,消耗高锰酸钾物质的量:
2KMnO4+3MnSO4+2H2O=5MnO2↓+K2SO4+2H2SO4,
2 5
n 0.23mol
n=0.0.092mol
为达到较好的除铁效果,每1L溶液应加入高锰酸钾的物质的量=0.092mol+0.01mol=0102mol;
故答案为:2KMnO4+3MnSO4+2H2O=5MnO2↓+K2SO4+2H2SO4;0.102mol;
(3)铁离子易发生水解反应生成氢氧化铁,当调节溶液PH,使溶液PH增大时,易使铁离子转化为氢氧化铁沉淀除去,
故答案为:使铁离子转化为氢氧化铁沉淀除去;
(4)根据题中信息,反应一段时间,二氧化锰和Fe (OH) 3发生吸附共沉作用,可知操作1为过滤,操作2为过滤后,滤液蒸发浓缩,冷却结晶,过滤洗涤;
故答案为:过滤,蒸发浓缩,冷却结晶,过滤洗涤;
(5)A.如果溶液的碱性太强,会与硫酸铝反应生成氢氧化铝沉淀而导致产率较低,故A错误;
B.活性二氧化锰不足时不能完全除去氢氧化铁,铁的去除率较低,过量时会增加成本,故B正确;
C.直接向溶液中加入二氧化锰粉末吸附作用太低,故C错误.
故答案为:B.
点评:本题考查较为综合,设计物质的制备流程、离子方程式的书写、氧化还原反应、物质的分离和提纯等问题,但题目难度中等,本题注意把握制备原理和实验流程.

练习册系列答案
相关题目
下列说法错误的是( )
| A、浓氨水可检验氯气管道泄漏 |
| B、明矾可用作除去污水中悬浮颗粒的絮凝剂 |
| C、Si和SiO2都用于制造光导纤维 |
| D、硬铝、青铜和不锈钢都属合金 |


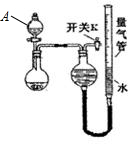

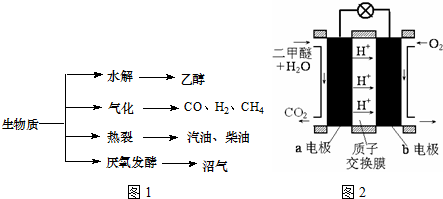
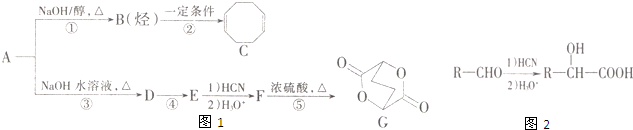
 (1)某学习小组用0.80mol/L标准浓度的烧碱溶液测定未知浓度的盐酸.
(1)某学习小组用0.80mol/L标准浓度的烧碱溶液测定未知浓度的盐酸.