题目内容
16.关于恒容密闭容器进行的反应C(s)+CO2(g)?2CO(g)△H>0.下列说怯不正确的是( )| A. | △s>0 | |
| B. | 在低温下能自发进行 | |
| C. | 当混合气体的密度不再变化时.反应达到平衡 | |
| D. | 达到平衡时,升高温度,CO2的转化率和反应速率均增大 |
分析 A.反应物气体的计量数小于生成物气体的计量数,熵变增大;
B.如能自发进行,应满足△H-T•△S<0;
C.有固体参加反应,如气体的密度不变,可说明达到平衡状态;
D.正反应吸热,升高温度,平衡正向移动.
解答 解:A.反应物气体的计量数小于生成物气体的计量数,熵变增大,则△s>0,故A正确;
B.△H>0,△s>0,如在低温下,△H-T•△S>0时,反应不能自发进行,故B错误;
C.有固体参加反应,如气体的密度不变,可说明达到平衡状态,故C正确;
D.正反应吸热,升高温度,反应速率增大,且平衡正向移动,二氧化碳的转化率增大,故D正确.
故选B.
点评 本题考查化学平衡影响因素,为高频考点,侧重考查学生分析判断能力,明确温度、压强、浓度对化学平衡影响原理是解本题关键题目难度不大.

练习册系列答案
相关题目
7.已知汽车尾气无害化处理反应为2NO(g)+2CO(g)?N2(g)+2CO2(g),下列说法中不正确的是( )
| A. | NO的消耗速率等于CO2的生成速率时,反应不一定达到平衡 | |
| B. | CO的消耗速率是N2消耗速率的两倍时达到平衡 | |
| C. | 反应达到平衡后,NO的浓度等于CO2的浓度 | |
| D. | 单位时间内消耗CO和CO2的物质的量相等时,反应达到平衡 |
8.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 常温常压下,64g SO2气体中所含分子数为NA | |
| B. | 标准状况下,4.48L四氯化碳中所含原子总数为NA | |
| C. | 1mol HNO3作氧化剂时转移电子数为3NA | |
| D. | 常温常压下,11.2L NO2中所含分子数为0.5NA |
5.设NA为阿伏伽德罗常数值.下列有关叙述正确的是( )
| A. | 电解精炼粗铜(含有锌铁等杂质),若阳极溶解32g铜,转移电子数目为NA | |
| B. | 256gS8(分子结构如图)含S-S键数为7NA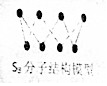 | |
| C. | 某温度下,pH=1的1LH2SO4溶液中含有的H+数目为0.1NA | |
| D. | 氢氧燃料电池正极消耗22.4L气体时,负极消耗的气体分子数目为2NA |

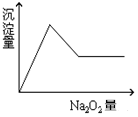 某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.
某溶液中可能含有下列8种离子中的一种或几种:H+、Na+、Cu2+、Mg2+、Al3+、NH4+、CO32-、Cl-.向该溶液中加入Na2O2固体放出一种无色无味的气体且产生白色沉淀,沉淀的量随加入Na2O2的量变化关系如图所示.试对该溶液中离子组成情况作出判断.


