题目内容
4.设NA为阿伏加德罗常数值,下列叙述正确的是( )| A. | 46gNO2和N2O4混合气体中氮原子数为NA | |
| B. | 1mol 14C含有的中子数为6NA | |
| C. | 标准状况下,22.4LCCl4中含有的分子数为NA | |
| D. | 0.5molNa2O2与足量水反应,转移电子数为NA |
分析 A、NO2和N2O4的最简式均为NO2;
B、14C中的质量数为14,质子数为6;
C、标况下四氯化碳为液体;
D、过氧化钠和水反应时,1mol过氧化钠转移1mol电子.
解答 解:A、NO2和N2O4的最简式均为NO2,故46g混合物中含有的NO2的物质的量为1mol,则含NA个氮原子,故A正确;
B、14C中的质量数为14,质子数为6,故中子数N=质量数-质子数=14-6=8,1mol14C中含8NA个中子,故B错误;
C、标况下四氯化碳为液体,故不能根据气体摩尔体积来计算其物质的量,故C错误;
D、过氧化钠和水反应时,1mol过氧化钠转移1mol电子,故0.5mol 过氧化钠转移0.5NA个电子,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意公式的运用和物质的结构特点.

练习册系列答案
相关题目
14.与100mL 0.4mol•L-1NH4NO3溶液中的NO3-浓度相同的是( )
| A. | 400 mL 0.1 mol•L-1的KNO3溶液 | B. | 100 mL 0.4 mol•L-1的Ba(NO3)2溶液 | ||
| C. | 100 mL 0.2 mol•L-1的Mg(NO3)2溶液 | D. | 200 mL 0.1mol•L-1的Fe(NO3)3溶液 |
15.用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A. | 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 9.2g甲苯和丙三醇的混合物中,含氢原子数目为0.8NA | |
| C. | 用惰性电极电解1L浓度均为0.2mol/L的Cu(NO3)2和AgNO3的混合溶液,当有0.2NA个电子转移时,理论上阴极析出6.4g金属 | |
| D. | 电解精炼铜(粗铜含铁、锌、银、金杂质)时,每转移2NA个电子,阴极析出1 mol Cu |
12.下列物质中分子间能形成氢键的是( )
| A. | HBr | B. | H2S | C. | NH3 | D. | PH3 |
19.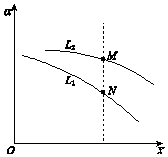 已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )
已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )
 已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )
已知:N2(g)+3H2(g)?2NH3(g)△H=-92kJ•mol-1,如图表示L一定时,H2的平衡转化率(α)随X的变化关系,L(L1、L2)、X可分别代表压强或温度.下列说法中,不正确的是( )| A. | X表示温度 | B. | L2>L1 | C. | 反应速率 υ(M)>υ(N) | D. | 平衡常数 K(M)>K(N) |
9. 我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )
我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )
 我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )
我国科研人员研制出一种室温“可呼吸”Na-CO2电池.放电时该电池“吸入”CO2,充电时“呼出”CO2.吸入CO2时,其工作原理如图所示.吸收的全部CO2中,有$\frac{2}{3}$转化为Na2CO3固体沉积在多壁碳纳米管(MWCNT)电极表面.下列说法正确的是( )| A. | “吸入”CO2时,钠箔为正极 | |
| B. | “呼出”CO2时,Na+向多壁碳纳米管电极移动 | |
| C. | “吸入”CO2时的正极反应:4Na++3CO2+4e-═2Na2CO3+C | |
| D. | 标准状况下,每“呼出”22.4 L CO2,转移电子数为0.75 mol |
16.化学反应中,反应物用量、浓度或反应条件不同可能对生成物产生影响.下列反应的生成物不受上述因素影响的是( )
| A. | 铜与硝酸反应 | B. | 钠与氧气反应 | ||
| C. | 氢气与氯气反应 | D. | 氯化铝与氢氧化钠溶液反应 |
13.乙烷混有乙烯,欲除去乙烯得到纯净干燥的乙烷,下列方法正确的( )
| A. | 依次通过溴水、烧碱、浓硫酸 | B. | 依次通过酸性KMnO4溶液、浓硫酸 | ||
| C. | 依次通过澄清石灰水、浓硫酸 | D. | 通入氢气,在一定条件下反应 |
14.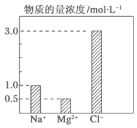 在2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,则此溶液中Ca2+离子的物质的量是( )
在2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,则此溶液中Ca2+离子的物质的量是( )
 在2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,则此溶液中Ca2+离子的物质的量是( )
在2L由NaCl、MgCl2、CaCl2组成的混合液中,部分离子浓度大小如图所示,则此溶液中Ca2+离子的物质的量是( )| A. | 0.5 mol | B. | 1.0 mol | C. | 2.0 mol | D. | 3.0 mol |