题目内容
2.下列说法中错误的是( )| A. | 在豆浆里加入盐卤做豆腐,在河流入海处易形成沙洲都与胶体性质有关 | |
| B. | 淀粉胶体中混有的氯化钠可以通过渗析的方法除去 | |
| C. | 一束平行光线射入蛋白质溶液里,从侧面可以看到一条光亮的通路 | |
| D. | Fe(OH)3悬浊液和Fe(OH)3胶体都不稳定,都不能透过滤纸 |
分析 A.豆浆具有胶体的性质;
B.离子可透过半透膜,而胶体不能;
C.蛋白质溶液是胶体;
D.胶体能透过滤纸,浊液不能透过滤纸.
解答 解:A.豆浆具有胶体的性质,向其中加入盐卤,盐卤中含丰富的电解质氯化钙等,可以使豆浆凝聚,与胶体有关,故A正确;
B.离子可透过半透膜,而胶体不能,则渗析法可除去淀粉中的氯化钠,故B正确;
C.蛋白质溶液是胶体,胶体能产生丁达尔效应,故C正确;
D.胶体能透过滤纸,浊液不能透过滤纸,用滤纸能分离胶体和悬浊液,故D错误.
故选D.
点评 本题考查胶体的性质,难度不大,明确胶体常见的性质有丁达尔现象、胶体的聚沉、渗析等,利用胶体性质对生产生活中实际问题进行解释.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
9.下列说法正确的是( )
| A. | 加热才能发生的反应一定是吸热反应 | |
| B. | 化学反应的热效应的大小与参加反应的物质的多少无关 | |
| C. | 反应物的总能量大于生成物的总能量的反应一定是放热反应 | |
| D. | 同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 |
10.下列叙述正确的是( )
| A. |  和 和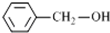 互为同系物 互为同系物 | |
| B. | 配制FeSO4溶液时,需加入少量铁粉和稀盐酸,既防止氧化又抑制水解 | |
| C. | 活化分子之间的碰撞不一定都是有效碰撞反应 | |
| D. | 对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,生成物的百分含量一定增加 |
7.下列各组物质相互混合反应后,最终有白色沉淀生成的是( )
①金属钠投入到FeCl2溶液中
②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中滴入少量盐酸
⑤向饱和Na2CO3通入足量CO2.
①金属钠投入到FeCl2溶液中
②过量NaOH溶液和明矾溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④向NaAlO2溶液中滴入少量盐酸
⑤向饱和Na2CO3通入足量CO2.
| A. | ①③④⑤ | B. | 只有①④ | C. | 只有②③ | D. | 只有③④⑤ |
14.常温下,下列有关0.1mol•L-1 Na2CO3溶液的说法正确的是( )
| A. | 升高温度,促进c(CO32-)水解,pH增大 | |
| B. | 离子浓度:c(Na+)=2[c(CO32-)+c(HCO3-)+c(H2CO3)] | |
| C. | 离子浓度:c(Na+)+c(H+)=c(CO32-)+c(HCO3-)+c(OH-) | |
| D. | 离子浓度:c(Na+)>c(CO32-)>c(H+)>c(OH-)>c(HCO3-) |
14.用NA表示示阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 含有NA个原子的氢气在标准状况下的体积约为22.4L | |
| B. | 25℃,1.01×105Pa,64g SO2中含有的原子数为3NA | |
| C. | 40gNaOH溶解在1L水中,所制得的100mL溶液中含Na+数为0.1NA | |
| D. | 标准状况下,11.2LH2O含有的分子数为0.53NA |
11.烷烃 是由某单烯烃与H2加成后的产物,(不考虑烯烃的顺反异构)则这种单烯烃的结构可能有( )
是由某单烯烃与H2加成后的产物,(不考虑烯烃的顺反异构)则这种单烯烃的结构可能有( )
 是由某单烯烃与H2加成后的产物,(不考虑烯烃的顺反异构)则这种单烯烃的结构可能有( )
是由某单烯烃与H2加成后的产物,(不考虑烯烃的顺反异构)则这种单烯烃的结构可能有( )| A. | 4种 | B. | 5种 | C. | 7种 | D. | 9种 |
12.下列有关说法不正确的是( )
| A. | 二氧化硫气体能使溴水、品红溶液褪色 | |
| B. | 浓硫酸是一种干燥剂,能够干燥H2、SO2、O2、NH3等气体 | |
| C. | 丁达尔现象、明矾净水、入海处形成三角洲都与胶体性质有关 | |
| D. | 铝制品在生活中很普遍,不易腐蚀,是因为它在空气中形成了一层致密的氧化膜,保护了里面的单质铝 |