题目内容
18.X、Y、Z、W四种短周期元素的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族,下列叙述正确的是( )| A. | X只能形成一种氧化物 | |
| B. | 化合物YX比WX3的熔点高 | |
| C. | 元素W的最高价氧化物对应水化物的酸性比Z的弱 | |
| D. | 原子半径的大小顺序:r(X)<r(Y)<r(Z)<r(W) |
分析 X、Y、Z、W四种短周期元素的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,X只能为2个电子层,最外层电子数为6,X为O元素;Y原子的最外层只有2个电子,结合原子序数可知Y为Mg元素;Z单质可制成半导体材料,Z为Si,W与X属于同一主族,W为S,以此来解答.
解答 解:由上述分析可知,X为O,Y为Mg,Z为Si,W为S,
A.X为O,能与其它元素形成氧化物,故A错误;
B.MgO为离子晶体,SO3为分子晶体,离子键比分子间作用力强,化合物YX比WX3的熔点高,故B正确;
C.非金属性S>Si,则元素W的最高价氧化物对应水化物的酸性比Z的强,故C错误;
D.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径的大小顺序:r(X)<r(W)<r(Z)<r(Y),故D错误;
故选B.
点评 本题考查原子结构与元素周期律,为高频考点,把握原子序数、原子结构、元素的位置来推断元素为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
9.现有部分短周期元素的性质或原子结构如表:
(1)元素X在元素周期表中的位置第三周期ⅥA族;
(2)元素Z的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有离子键和共价键;
(3)元素X与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是de;
a.常温下X的单质和T的单质状态不同
b.X的氢化物比T的氢化物稳定
c.X的单质与H2化合比T的单质与H2化合更容易
d.T的单质可以把X单质从它的氢化物中置换出来
e.X的最高价氧化物所对应的水化物比T的最高价氧化物所对应的水化物的酸性弱
(4)写出T的单质与元素Y的最高价氧化物所对应的水化物反应的离子方程式2OH-+Cl2=Cl-+ClO-+H2O.
| 元素编号 | 元素性质或原子结构 |
| X | M层的电子数为K层电子数的3倍 |
| Y | 短周期中最活泼的金属元素 |
| Z | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| T | 元素最高正价是+7价 |
(2)元素Z的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有离子键和共价键;
(3)元素X与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是de;
a.常温下X的单质和T的单质状态不同
b.X的氢化物比T的氢化物稳定
c.X的单质与H2化合比T的单质与H2化合更容易
d.T的单质可以把X单质从它的氢化物中置换出来
e.X的最高价氧化物所对应的水化物比T的最高价氧化物所对应的水化物的酸性弱
(4)写出T的单质与元素Y的最高价氧化物所对应的水化物反应的离子方程式2OH-+Cl2=Cl-+ClO-+H2O.
6.X、Y、Z、W为原子序数依次递增的短周期主族元素,X、Y两元素的原子最外层电子数之和为10,且X、Y可形成两种气态化合物甲和乙;Y、Z能形成一种具有强氧化性的淡黄色固体化合物丙;W与X位于同一主族.下列说法正确的是( )
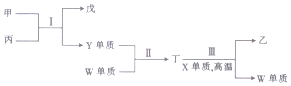

| A. | 原子半径:X<Y<Z | |
| B. | 反应Ⅰ中丙既能做氧化剂又作还原剂 | |
| C. | 非金属性:X>Y>W | |
| D. | 反应Ⅱ和Ⅲ反应均属于置换反应 |
13.下列说法正确的是( )
| A. | 向氨水中不断通入CO2,随着CO2的增加,$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$不断减小 | |
| B. | 在铜的精炼过程中,若转移1mol电子,则阳极一定溶解32gCu | |
| C. | 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)=4Fe(OH)3(s)△H>0,△S<0 | |
| D. | 将如图中的活塞快速推至A处固定,气体颜色先变深、再变浅,但比起始时深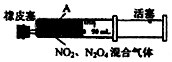 |
3.为了分离提纯蛋白质,不可在蛋白质溶液中加入下列试剂中的( )
| A. | 甲醛溶液 | B. | 饱和硫酸钠溶液 | C. | 硝酸铅溶液 | D. | 饱和硫酸铜溶液 |
10.下列说法中错误的是( )
| A. | 卤化氢中,以HF沸点最高,是由于HF分子间存在氢键 | |
| B. | 邻羟基苯甲醛的熔、沸点比对羟基苯甲醛的熔、沸点低 | |
| C. | H2O的沸点比HF的沸点高,是由于水中氢键键能大 | |
| D. | 氨气极易溶于水与氨气分子和水分子形成氢键有关 |
7.下列各组物质性质的比较中正确的是( )
| A. | 酸性:H3PO4>H2SO4>HClO4 | B. | 碱性:Mg(OH)2>Ca(OH)2>KOH | ||
| C. | 热稳定性:H2S>H2O>HF | D. | 氧化性:F2>Cl2>Br2>I2 |
8.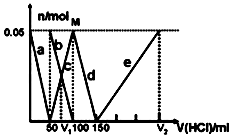 某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示.则下列说法正确的是( )
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示.则下列说法正确的是( )
(已知:H2CO3的电离平衡常数K1=4.3×10-7,K2=5.6×10-11;Al(OH)3的酸式电离平衡常数K=6.3×10-13)
 某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示.则下列说法正确的是( )
某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L-1的盐酸,测得溶液中的CO32-、HCO3-、AlO2-、Al3+的物质的量与加入盐酸溶液的体积变化关系如图所示.则下列说法正确的是( )(已知:H2CO3的电离平衡常数K1=4.3×10-7,K2=5.6×10-11;Al(OH)3的酸式电离平衡常数K=6.3×10-13)
| A. | a曲线表示的离子方程式为:AlO2-+4H+=Al3++2H2O | |
| B. | M点时生成的CO2为0.05mol | |
| C. | 原混合溶液中的CO32-与AlO2-的物质的量之比为1:2 | |
| D. | V1:V2=1:4 |