题目内容
短周期元素A、B、C、D原子序数依次增大,且只有C为金属元素,A、C位于同一主族,B的最外层电子数是次外层的3倍,B、C的最外层电子数之和与D的最外层电子数相等.
请回答下列问题:
(1)D的最高价氧化物对应的水化物名称为 .
(2)A2B2的电子式为 .
(3)由上述四种元素中的三种组成某种盐,水溶液呈碱性,是家用消毒剂的主要成分,将该溶液滴入KI淀粉溶液中,溶液变为蓝色,则反应的离子方程式为 .
(4)用石墨电极电解CD的饱和溶液,反应的离子方程式为 ,若反应后溶液的体积为200mL,常温下测得溶液的pH为13,则外电路中通过电子的物质的量为 .
(5)实验室欲检验CD溶液中所含的D-,其操作方法、现象和结论为 .
请回答下列问题:
(1)D的最高价氧化物对应的水化物名称为
(2)A2B2的电子式为
(3)由上述四种元素中的三种组成某种盐,水溶液呈碱性,是家用消毒剂的主要成分,将该溶液滴入KI淀粉溶液中,溶液变为蓝色,则反应的离子方程式为
(4)用石墨电极电解CD的饱和溶液,反应的离子方程式为
(5)实验室欲检验CD溶液中所含的D-,其操作方法、现象和结论为
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:只有C为金属元素,A、C同主族,所以A、C可能分别为H、Na,也可能为B、Al,B的最外层电子数是次外层电子数的3倍,B为O,如A为H元素,则C为Na元素,D的最外层电子数为1+6=7,应为Cl元素,合理,如A为B元素,则D的最外层电子数为3+6=9,不符合,所以A、B、C、D分别为H、O、Na、Cl元素,结合元素对应单质、化合物的结构和性质解答该题.
解答:
解:只有C为金属元素,A、C同主族,所以A、C可能分别为H、Na,也可能为B、Al,B的最外层电子数是次外层电子数的3倍,B为O,如A为H元素,则C为Na元素,D的最外层电子数为1+6=7,应为Cl元素,合理,如A为B元素,则D的最外层电子数为3+6=9,不符合,所以A、B、C、D分别为H、O、Na、Cl元素,则
(1)D为Cl元素,对应的最高价氧化物的水化物为高氯酸,故答案为:高氯酸;
(2)A2B2为H2O2,为共价化合物,其电子式为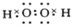 ,故答案为:
,故答案为: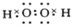 ;
;
(3)水溶液呈碱性的家用消毒剂为NaClO,具有强氧化性,与KI反应生成单质碘,反应的离子方程式为2I-+ClO-+H2O=I2+Cl-+2OH-,
故答案为:2I-+ClO-+H2O=I2+Cl-+2OH-;
(4)电解饱和食盐水,反应的离子方程式为2Cl-+2H2O
Cl2↑+H2↑+2OH-;阴极发生反应为2H++2e-=H2↑或2H2O+2e-=H2↑+2OH-,阳极反应为2Cl--2e-=Cl2↑,若反应后溶液的体积为200mL,测得pH为13,则n(e-)=n(OH-)=0.2L×0.1mol/L=0.02mol,
故答案为:2Cl-+2H2O
Cl2↑+H2↑+2OH-; 0.02mol;
(5)通常用硝酸酸化的AgNO3溶液检验NaCl溶液中Cl-,具体步骤为取适量NaCl溶液置于试管中,向其中滴入少量,若产生白色沉淀,则证明有Cl-,故答案为:取适量NaCl溶液置于试管中,向其中滴入少量,若产生白色沉淀,则证明有Cl-.
(1)D为Cl元素,对应的最高价氧化物的水化物为高氯酸,故答案为:高氯酸;
(2)A2B2为H2O2,为共价化合物,其电子式为
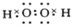 ,故答案为:
,故答案为: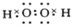 ;
;(3)水溶液呈碱性的家用消毒剂为NaClO,具有强氧化性,与KI反应生成单质碘,反应的离子方程式为2I-+ClO-+H2O=I2+Cl-+2OH-,
故答案为:2I-+ClO-+H2O=I2+Cl-+2OH-;
(4)电解饱和食盐水,反应的离子方程式为2Cl-+2H2O
| ||
故答案为:2Cl-+2H2O
| ||
(5)通常用硝酸酸化的AgNO3溶液检验NaCl溶液中Cl-,具体步骤为取适量NaCl溶液置于试管中,向其中滴入少量,若产生白色沉淀,则证明有Cl-,故答案为:取适量NaCl溶液置于试管中,向其中滴入少量,若产生白色沉淀,则证明有Cl-.
点评:本题考查原子结构以及元素周期律知识,题目难度中等,本题注意短周期元素既有金属又有非金属的主族有H、Li、Na以及B、Al等,注意B、C的最外层电子数之和与D的最外层电子数相等.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目
在可逆反应2A(g)+3B(g)?xC(g)+D(g)中,起始浓度A为5mol?L-1,B为3mol?L-1,C的反应速率为0.5mol?(L?min)-1,2min后,测得D的浓度为0.5mol?L-1.则关于此反应的下列说法中正确的是( )
| A、2 min末时,A和B的浓度之比为5:3 |
| B、x=1 |
| C、2 min末时,B的浓度为1.5 mol?L-1 |
| D、2 min末时,A的消耗浓度为0.5 mol?L-1 |
下列对物质的分类不正确的是( )
| A、H2SO4-酸 |
| B、NaOH-碱 |
| C、HClO-氧化物 |
| D、KI-盐 |

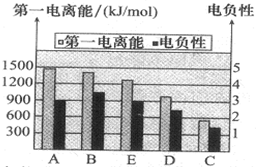 A、B、C、D、E是原子序数依次增大的五种短周期元素,其有关性质或结构信息如表所示:
A、B、C、D、E是原子序数依次增大的五种短周期元素,其有关性质或结构信息如表所示: