题目内容
13.下列说法正确的是( )| A. | 葡萄糖的燃烧热是2800 kJ•mol-1,则$\frac{1}{2}$C6H12O6(s)+3O2(g)═3CO2(g)+3H2O(l)△H=-1400 kJ•mol-1 | |
| B. | 已知101 kPa时,2C(s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则该反应的反应热为221 kJ•mol-1 | |
| C. | 已知稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,则稀醋酸与稀氢氧化钠溶液反应生成1 mol水时放出57.3 kJ的热量 | |
| D. | 已知HCl和NaOH反应的中和热△H=-57.3 kJ•mol-1,则98%的浓硫酸与稀氢氧化钠溶液反应生成1 mol水的中和热为-57.3 kJ•mol-1 |
分析 A.根据燃烧热的定义判断热化学方程式;
B.应指明反应为吸热反应还是放热反应;
C.醋酸为弱酸,电离吸热;
D.浓硫酸溶于水放热.
解答 解:A.燃烧热是指完全反应生成稳定的氧化物,生成的水为液态,所以葡萄糖的燃烧热是2800 kJ•mol-1,则$\frac{1}{2}$C6H12O6(s)+3O2(g)═3CO2(g)+3H2O(l)△H=-1400 kJ•mol-1,故A正确;
B.应指明反应为吸热反应还是放热反应,故B错误;
C.醋酸为弱酸,电离吸热,则稀醋酸与稀氢氧化钠溶液反应生成1 mol水时放出的热量小于57.3 kJ,故C错误;
D.浓硫酸溶于水放热,则98%的浓硫酸与稀氢氧化钠溶液反应生成1 mol水的中和热小于-57.3 kJ•mol-1,故D错误.
故选A.
点评 本题考查学生对热化学方程式的理解、反应热与能量关系,为高频考点,侧重考查学生的分析能力,注意把握燃烧热、中和热等定义的理解,难度不大,把握热化学方程式的书写方法.

练习册系列答案
相关题目
3.某固体A在一定条件下加热分解,产物全是气体.A的分解反应为:2A$\frac{\underline{\;\;△\;\;}}{\;}$B+2C+2D,现测得分解产生的混合气体的密度是氢气的d倍,则A的相对分子量为( )
| A. | 2d | B. | 2.5d | C. | 5d | D. | 0.8d |
18.下列物质的分类正确的是( )
| 单质 | 氧化物 | 酸 | 碱 | 盐 | |
| A | 钠 | 水 | 硝酸 | 小苏打 | 胆矾 |
| B | 生铁 | 硅酸钠 | H2SiO3 | KOH | NH4Cl |
| C | 晶体硅 | 过氧化钠 | 盐酸 | '纯碱 | 明矾 |
| D | 液氯 | 铁红 | 硫酸 | Ca(OH)2 | Na2SO4 |
| A. | A | B. | B | C. | C | D. | D |
5.下列有关热化学方程式及其叙述正确的是( )
| A. | 氢气的燃烧热为285.5 kJ•mol-1,则水分解的热化学方程式为2H2O(l)═2H2(g)+O2(g)△H=+285.5 kJ•mol-1 | |
| B. | 已知2C(石墨,s)+O2(g)═2CO(g)△H=-221 kJ•mol-1,则石墨的燃烧热为 110.5 kJ•mol-1 | |
| C. | 已知N2(g)+3H2(g)?2NH3(g)△H=-92.4 kJ•mol-1,则在一定条件下将1 mol N2和3 mol H2置于一密闭容器中充分反应后最多可放出92.4 kJ的热量 | |
| D. | 已知乙醇和乙烯的燃烧热分别为1 366.8 kJ•mol-1和1 411.0 kJ•mol-1,则乙烯水化制乙醇的热化学方程式为C2H4(g)+H2O(l)═C2H5OH(l)△H=-44.2 kJ•mol-1 |
2.常温下,用0.1mol/L的盐酸滴定a mL NaOH稀溶液.反应恰好完全时,消耗盐酸b mL.此时溶液时中c (OH-)是( )
| A. | 1.0×10-7 mol/L | B. | 1.0×107 mol/L | C. | $\frac{0.1}{a}$mol/L | D. | $\frac{0.1b}{a+b}$mol/L |
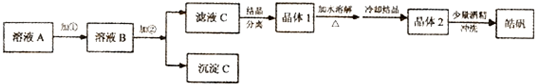
1.实验化学实验室通常用粗锌和稀硫酸反应制氢气,因此在制氢废液中含有大量的硫酸锌.同时,由于粗锌中还含有铁等杂质,使得溶液中混有一定量的硫酸亚铁,为了充分利用制氢废液,常用其制备皓矾(ZnSO4•7H2O).某校化学兴趣小组的同学以制氢气的废液为原料来制取皓矾并探究其性质.
(l)制备皓矾的实验流程如图所示.
已知:下列氢氧化物开始生成沉淀到沉淀完全的pH范围分别为:
回答下列问题:
可供选择使用的有:氯水、20%的H2O2、氨水、NaOH溶液、Zn(OH)2、ZnO
①加入的试剂①,应选用20%的H2O2,发生反应的离子方程式为2H++H2O2+2Fe2+=2Fe3++2H2O
②加入的试剂②,可选用ZnO或Zn(OH)2,其作用是调节溶液的pH至3.7-5.7,使Fe3+完全转化为Fe(OH)3沉淀,同时避免引入新的杂质
③从晶体l→晶体2,该提纯过程的名称是重结晶.
④有同学提出,应将晶体1加入稀硫酸中溶解,请结合离子方程式解析Zn2++2H2O?Zn(OH)2+2H+,稀硫酸可抑制ZnSO4的水解,防止产生Zn(OH)2杂质.
⑤在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是为了冲洗掉晶体表面残留的滤液,防止晶体溶解,影响产率.
(2)检验皓矾中是否含有Fe元素的操作(试剂自选)取少量皓矾溶于水配制成溶液,往所得溶液中滴加适量KSCN溶液,如无明显现象说明不含Fe3+,如溶液变为红色则说明含Fe3+.
(l)制备皓矾的实验流程如图所示.

已知:下列氢氧化物开始生成沉淀到沉淀完全的pH范围分别为:
| 开始沉淀 | 沉淀完全 | |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6 |
| Zn(OH)2 | 5.7 | 8.0 |
可供选择使用的有:氯水、20%的H2O2、氨水、NaOH溶液、Zn(OH)2、ZnO
①加入的试剂①,应选用20%的H2O2,发生反应的离子方程式为2H++H2O2+2Fe2+=2Fe3++2H2O
②加入的试剂②,可选用ZnO或Zn(OH)2,其作用是调节溶液的pH至3.7-5.7,使Fe3+完全转化为Fe(OH)3沉淀,同时避免引入新的杂质
③从晶体l→晶体2,该提纯过程的名称是重结晶.
④有同学提出,应将晶体1加入稀硫酸中溶解,请结合离子方程式解析Zn2++2H2O?Zn(OH)2+2H+,稀硫酸可抑制ZnSO4的水解,防止产生Zn(OH)2杂质.
⑤在得到皓矾时,向晶体中加入少量酒精洗涤而不用水的原因是为了冲洗掉晶体表面残留的滤液,防止晶体溶解,影响产率.
(2)检验皓矾中是否含有Fe元素的操作(试剂自选)取少量皓矾溶于水配制成溶液,往所得溶液中滴加适量KSCN溶液,如无明显现象说明不含Fe3+,如溶液变为红色则说明含Fe3+.
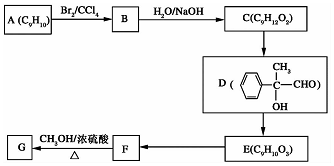
 .
.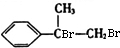 +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$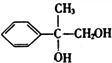 +2NaBr
+2NaBr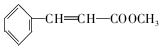 互为同分异构体
互为同分异构体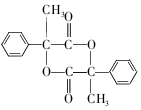 合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3.
合成路线流程图示例如下:CH3CH2Br$→_{△}^{NaOH溶液}$CH3CH2OH$→_{浓硫酸,△}^{CH_{3}COOH}$CH3COOCH2CH3.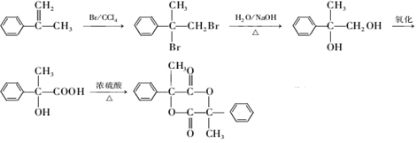 .
.