题目内容
下列叙述中正确的是( )
| A、干燥的NaCl晶体不能导电,所以它不是电解质 |
| B、食盐水能导电,所以食盐水是电解质 |
| C、食盐水通电时可电离出Na+和Cl- |
| D、食盐水溶液呈电中性 |
考点:电解质与非电解质,电解质溶液的导电性
专题:离子反应专题
分析:A.电解质在水溶液或熔融状态下能导电;
B.食盐水是混合物,电解质是化合物;
C.电离不是在通电后才发生的,而是在溶于水或熔融时发生;
D.电解质溶液中阴阳离子所带的电荷数相等,溶液呈电中性.
B.食盐水是混合物,电解质是化合物;
C.电离不是在通电后才发生的,而是在溶于水或熔融时发生;
D.电解质溶液中阴阳离子所带的电荷数相等,溶液呈电中性.
解答:
解:A.固态氯化钠不导电,但在水溶液或熔融状态下能导电,属于电解质,故A错误;
B.食盐水是混合物,不是化合物,不属于电解质,故B错误;
C.电离不是在通电后才发生的,而是在溶于水或熔融时发生的,故C错误;
D.电解质溶液中虽然有阴阳离子,但阴阳离子所带的电荷数相等,故溶液呈电中性,故D正确;
故选:D.
B.食盐水是混合物,不是化合物,不属于电解质,故B错误;
C.电离不是在通电后才发生的,而是在溶于水或熔融时发生的,故C错误;
D.电解质溶液中虽然有阴阳离子,但阴阳离子所带的电荷数相等,故溶液呈电中性,故D正确;
故选:D.
点评:本题考查电解质、非电解质的定义、物质导电的原因,题目难度不大,注意能导电的不一定是电解质,如硝酸钾溶液;电解质不一定能导电,如固态氯化钾.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
在某一化学反应A+2B?3C中,生成物B的浓度在10s内从1.5mol/L变成2.0mol/L,则这10s内用生成物C的浓度变化表示的化学反应速率为( )
| A、0.05mol/(L?s) |
| B、0.05mol/L |
| C、0.033 mol/(L?s) |
| D、0.075 mol/(L?s) |
下列离子方程式中正确的是( )
| A、NaHSO4溶液和Ba(OH)2溶液充分反应后溶液呈中性:Ba2++2OH-+2H++SO4_2-=BaSO4↓+2H2O |
| B、向NH4Al(SO4)2溶液中滴入Ba(OH)2恰好使SO42-反应完全:2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
| C、次氯酸钠溶液中通入SO2气体:2ClO-+SO2+H2O═2HClO+SO42- |
| D、Fe(OH)3溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
有aXm+和bYn-两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是( )
| A、b-a=n+m |
| B、a-b=n+m |
| C、核电荷数Y=X |
| D、核电荷数Y>X |
设C+CO2?2CO;(正反应为吸热反应;反应速率为v1),2SO2+O2?2SO3;(正反应为放热反应;反应速率为v2),对于上述反应,当温度升高时,v1和v2的变化情况为( )
| A、v1 与v2同时增大 |
| B、v1 与v2同时减小 |
| C、v1增大,v2减小 |
| D、v1减小,v2增大 |
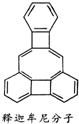 美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子就像一尊释迦牟尼佛,因而称为释迦牟尼分子(所有原子在同一平面),其结构简式如图所示.有关该有机分子的下列说法正确的是( )
美国康乃尔大学的魏考克斯(C.Wilcox)所合成的一种有机分子就像一尊释迦牟尼佛,因而称为释迦牟尼分子(所有原子在同一平面),其结构简式如图所示.有关该有机分子的下列说法正确的是( )| A、该有机物属于芳香烃 |
| B、该有机物属于苯的同系物 |
| C、该有机物分子中含有22个碳原子和22个氢原子 |
| D、该有机物的一氯代物只有3种 |
下列描述的一定是金属元素的是( )
| A、易失去电子的物质 |
| B、能与酸反应的物质 |
| C、原子最外电子层只有一个电子的元素 |
| D、原子核内有11个质子的元素 |
下列关于能源和作为能源物质的叙述中错误的是( )
| A、燃料燃烧时将化学能全部转化为热能 |
| B、绿色植物进行光合作用时,将太阳能转化为化学能“贮存”起来 |
| C、物质的化学能可以在不同条件下转为热能、电能为人类所利用 |
| D、化石燃料蕴藏的能量来自远古时期生物体所吸收利用的太阳能 |
X、Y、Z三种元素位于周期表中同一周期,其最高价氧化物分别为酸性氧化物、碱性氧化物、两性氧化物,则这三种元素原子序数的大小顺序是( )
| A、X>Y>Z |
| B、X>Z>Y |
| C、Y>X>Z |
| D、Y>Z>X |