题目内容
1.某有机物的结构简式如图,下列关于该有机物的叙述中不正确的是( )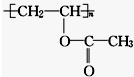
| A. | 1 mol 该有机物与 NaOH 溶液完全反应时,消耗 1 mol NaOH | |
| B. | 该有机物水解所得产物能发生酯化反应 | |
| C. | 该有机物可通过加聚反应生成 | |
| D. | 该有机物属于混合物 |
分析 由结构简式可知,分子中含n个-COOC-,结合酯的性质来解答.
解答 解:A.分子中含n个-COOC-,1mol该有机物与NaOH溶液完全反应时,消耗NaOH nmol,故A错误;
B.水解反应生成聚乙烯醇和乙酸,含有羟基和羧基,可发生酯化反应,故B正确;
C.高分子主链只有2个C,为加聚反应产物,该有机物可通过加聚反应生成,故C正确;
D.为高聚物,n介于较大范围之间,没有确定的值,则该有机物为混合物,故D正确.
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重酯、烯烃性质的考查,注意聚合度的分析,题目难度不大.

练习册系列答案
相关题目
12.下列关于钠与水反应的说法不正确的是( )
①将一小块钠投入滴有石蕊试液的水中,反应后溶液变蓝
②将钠投入稀盐酸中,钠先与水反应,后与盐酸反应
③钠在水蒸气中反应时因温度高会燃烧
④将两小块质量相等的金属钠,一块直接投入水中,另一块用铝箔包住,在铝箔上刺些小孔,然后按入水中,两者放出的氢气质量相等.
①将一小块钠投入滴有石蕊试液的水中,反应后溶液变蓝
②将钠投入稀盐酸中,钠先与水反应,后与盐酸反应
③钠在水蒸气中反应时因温度高会燃烧
④将两小块质量相等的金属钠,一块直接投入水中,另一块用铝箔包住,在铝箔上刺些小孔,然后按入水中,两者放出的氢气质量相等.
| A. | ①② | B. | ①②③ | C. | ②③④ | D. | ①②③④ |
9.下列离子方程式中,正确的是( )
| A. | 氯化铁溶液腐蚀印刷线路板:Fe3++Cu=Fe2++Cu2+ | |
| B. | 将少量铜屑放入浓硝酸中:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O | |
| C. | 钠和水反应:Na+2H2O=Na++2OH-+H2↑ | |
| D. | 碳酸氢钠溶液与盐酸反应:CO32-+2H+=CO2↑+H2O |
6.已知常温下浓度为0.1mol•L-1的下列溶液的pH如表所示:
下列有关说法正确的是( )
| 溶质 | NaF | NaClO | Na2CO3 |
| pH | 7.5 | 9.7 | 11.6 |
| A. | 0.1 mol•L-1 Na2CO3溶液中,存在关系:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) | |
| B. | 加热0.1 mol•L-1 NaClO溶液测其pH,pH小于9.7 | |
| C. | pH=2的HF溶液与pH=12的NaOH溶液以等体积混合,则有c(Na+)=c(F-)>c(H+)=c(OH-) | |
| D. | 根据上表数据得出三种酸电离平衡常数大小关系为:HF>HClO>H2CO3(一级电离平衡常数) |
13. 污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
实验仪器
I.实验原理:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O.
Ⅱ.实验设计
(1)【方案】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4
溶液混合后,溶液褪色所需的时间.拟定实验数据:
表中①、②处的数据分别是25、7.0.
III.讨论与交流
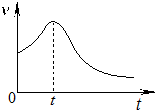
(2)小组同学在处理一系列的实验数据时,发现速率(v)-时间(t)曲线如图所示.他们认为:0~t时间内,速率变快的可能原因是①产物Mn2+是反应的催化剂、②该反应放热使温度升高.
(3)实验室常用KMnO4标准溶液滴定某浓度草酸.
KMnO4溶液置于酸式滴定管(填仪器名称)中,判断到达滴定终点的现象是溶液由无色变为浅紫红色,且半分钟内不褪色.若读取滴定管数据时,起始读数正确,终点俯视读数,则测定结果偏低(填“偏高”、“偏低”、“无影响”).
 污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.
污鸡净的主要成分是KMnO4和H2C2O4,可用于洗涤有霉斑的衣物.某小组同学拟探究H2C2O4浓度对反应速率的影响.实验仪器
I.实验原理:2KMnO4+5H2C2O4+3H2SO4═K2SO4+2MnSO4+10CO2↑+8H2O.
Ⅱ.实验设计
(1)【方案】观察反应现象:在其它相同条件下,测定不同浓度H2C2O4溶液与等体积等浓度KMnO4
溶液混合后,溶液褪色所需的时间.拟定实验数据:
| 实验序号 | 温度/℃ | 各物质的体积/mL | 反应时间 | |||
| H2O | 3mol/L稀硫酸 | 0.1mol/L KMnO4溶液 | 0.6mol/LH2C2O4溶液 | |||
| 1 | 25 | 3.0 | 2.0 | 4.0 | 6.0 | t1 |
| 2 | ① | 5.0 | 2.0 | 4.0 | 4.0 | t2 |
| 3 | 25 | ② | 2.0 | 4.0 | 2.0 | t3 |
III.讨论与交流
(2)小组同学在处理一系列的实验数据时,发现速率(v)-时间(t)曲线如图所示.他们认为:0~t时间内,速率变快的可能原因是①产物Mn2+是反应的催化剂、②该反应放热使温度升高.
(3)实验室常用KMnO4标准溶液滴定某浓度草酸.
KMnO4溶液置于酸式滴定管(填仪器名称)中,判断到达滴定终点的现象是溶液由无色变为浅紫红色,且半分钟内不褪色.若读取滴定管数据时,起始读数正确,终点俯视读数,则测定结果偏低(填“偏高”、“偏低”、“无影响”).
 (1)图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.
(1)图是1mol NO2和1mol CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:NO2(g)+CO(g)=CO2(g)+NO(g)△H=-234kJ•mol-1.
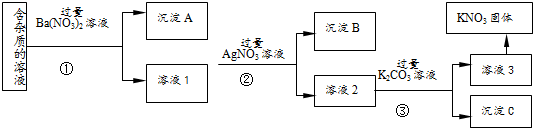
 现有含有少量KCl、K2SO4、K2CO3杂质的KNO3溶液,选择适当的试剂除去杂质,得到纯净的KNO3固体,实验流程如图所示.
现有含有少量KCl、K2SO4、K2CO3杂质的KNO3溶液,选择适当的试剂除去杂质,得到纯净的KNO3固体,实验流程如图所示.