题目内容
13.①相同物质的量的SO2和SO3,含氧原子个数比为2:3 它们的质量之比为4:5②相同质量的SO2和SO3,物质的量之比为5:4.
分析 ①结合n=$\frac{N}{{N}_{A}}$=$\frac{m}{M}$以及物质的构成计算;
②已知M(SO2)=64g/mol,M(SO3)=80g/mol,结合n=$\frac{m}{M}$计算.
解答 解:①设物质的量都为1mol,
所含氧原子的物质的量之比为2:3,含氧原子个数比为2:3,
m(SO2)=1mol×64g/mol=64g,m(SO3)=1mol×80g/mol=80g,它们的质量之比为64:80=4:5,
故答案为:2:3;4:5;
②已知M(SO2)=64g/mol,M(SO3)=80g/mol,由n=$\frac{m}{M}$可知,物质的量与摩尔质量成反应比,即80:64=5:4,故答案为:5:4.
点评 本题考查物质的量的计算,侧重于学生的分析能力能力和计算能力的考查,为高频考点,注意把握原子构成以及相关物理量的计算公式的运用,难度不大.

练习册系列答案
相关题目
4.生活环境逐渐恶化,人们日益重视环境问题,下列做法或说法正确的是( )
| A. | 推广使用无磷洗衣粉,以减少水体富营养化 | |
| B. | PM2.5是指大气中直径接近于2.5μm(1m=106μm=109nm)的颗粒物,也称可吸入颗粒物,这些细颗粒物分散在空气中形成的分散系是胶体 | |
| C. | 为提高农作物产量大量使用农药和化肥 | |
| D. | 对农作物秸秆进行焚烧还田,以增加土壤肥力 |
1.在1mol Al2(SO4)3中含有的Al3+个数约是( )
| A. | 6.02×1023 | B. | 1.204×1024 | C. | 2 | D. | 1 |
8.随着科技的不断进步,15N、N70、N5+、NH5等已被发现.下列有关说法中,正确的是( )
| A. | 15N中含有7个中子 | |
| B. | N2和N70属于同位素 | |
| C. | N5+中含有36个电子 | |
| D. | 若NH5为离子化合物,则其既含有离子键,又含有共价 |
18.下列混合物的分离和提纯方法中,主要不是从物质的溶解性角度考虑的是( )
| A. | 过滤 | B. | 蒸馏 | C. | 结晶 | D. | 萃取 |
5.下列化学用语应用正确的是( )
| A. | 乙烯的结构简式:CH2CH2 | B. | 乙醇的分子式:CH3CH2OH | ||
| C. | 甲烷的结构式:CH4 | D. | 甲苯的键线式: |
11. 恒温下,向一个4L的密闭容器中充入5.2molH2和2molN2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
恒温下,向一个4L的密闭容器中充入5.2molH2和2molN2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
①下列可以证明反应达到平衡的标志是ACDF.
A.N2、H2和NH3的浓度不再变化
B.单位时间内消耗n mol N2同时消耗3nmol H2
C.1mol氮氮三键断裂同时6molN-H键断裂
D.容器内总压强不随时间而变化
E.混合气体的密度保持不变
F.混合气体的平均相对分子质量不再改变
②此条件下该反应的化学平衡常数K=0.1,若温度不变,只将容器体积由4L变为2L,达到新平衡时N2的平衡浓度>0.4mol•L-1(填“>”、“=”或“<”).
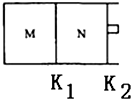
③如图所示,隔板K1固定不动,活塞K2可自由移动.T℃时,M、N两个容器中均发生反应N2(g)+3H2(g)?2NH3(g),向容器M、N中各充入l mol N2和3mol H2,初始M、N的容积和温度相同,并保持温度不变.下列有关说法中不正确的是A.
A.反应达到平衡时N2的转化率:M>N
B.H2的体积分数:M>N
C.容器N中达到平衡,测得容器中含有1.2mol NH3,此时N的容积为VL,则该反应在此条件下的平衡常数K=
$\frac{24{V}^{2}}{12}$
D.该反应在T℃时的平衡常数K:M=N.
 恒温下,向一个4L的密闭容器中充入5.2molH2和2molN2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:
恒温下,向一个4L的密闭容器中充入5.2molH2和2molN2,反应过程中对NH3的浓度进行检测,得到的数据如表所示:| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol•L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
A.N2、H2和NH3的浓度不再变化
B.单位时间内消耗n mol N2同时消耗3nmol H2
C.1mol氮氮三键断裂同时6molN-H键断裂
D.容器内总压强不随时间而变化
E.混合气体的密度保持不变
F.混合气体的平均相对分子质量不再改变
②此条件下该反应的化学平衡常数K=0.1,若温度不变,只将容器体积由4L变为2L,达到新平衡时N2的平衡浓度>0.4mol•L-1(填“>”、“=”或“<”).
③如图所示,隔板K1固定不动,活塞K2可自由移动.T℃时,M、N两个容器中均发生反应N2(g)+3H2(g)?2NH3(g),向容器M、N中各充入l mol N2和3mol H2,初始M、N的容积和温度相同,并保持温度不变.下列有关说法中不正确的是A.
A.反应达到平衡时N2的转化率:M>N
B.H2的体积分数:M>N
C.容器N中达到平衡,测得容器中含有1.2mol NH3,此时N的容积为VL,则该反应在此条件下的平衡常数K=
$\frac{24{V}^{2}}{12}$
D.该反应在T℃时的平衡常数K:M=N.
12.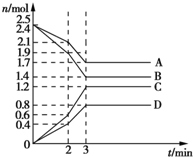 在某容积为2L的密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化如图所示.下列说法正确的是( )
在某容积为2L的密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化如图所示.下列说法正确的是( )
 在某容积为2L的密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化如图所示.下列说法正确的是( )
在某容积为2L的密闭容器中,A、B、C、D四种气体物质发生可逆反应,其物质的量n(mol)随时间t(min)的变化如图所示.下列说法正确的是( )| A. | 前2min内,v(A)=0.2 mol/(L•min) | |
| B. | 在2min时,图象发生改变的原因只可能是增大压强 | |
| C. | 其他条件不变,3min时体系的压强不再发生变化 | |
| D. | 增加气体D的浓度,A的反应速率随之减小 |