题目内容
已知下列两个气态物质之间的反应:C2H2(g)+H2(g)?C2H4(g)…①,
2CH4(g)?C2H4(g)+2H2(g)…②.
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
C(s)+2H2(g)?CH4(g),△H=-Q1…Ⅰ
C(s)+
H2(g)?
C2H2(g),△H=-Q2…Ⅱ
C(s)+H2(g)?
C2H4(g),△H=-Q3…Ⅲ(Q1、Q2、Q3均为正值),
“Q值”大小比较正确的是( )
2CH4(g)?C2H4(g)+2H2(g)…②.
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
C(s)+2H2(g)?CH4(g),△H=-Q1…Ⅰ
C(s)+
| 1 |
| 2 |
| 1 |
| 2 |
C(s)+H2(g)?
| 1 |
| 2 |
“Q值”大小比较正确的是( )
| A、Q1>Q3>Q2 |
| B、Q1>Q2>Q3 |
| C、Q2>Q1>Q3 |
| D、Q3>Q1>Q2 |
分析:先根据温度变化所引起平衡移动的方向判断反应①、反应②的热效应,然后利用盖斯定律判断即可.
解答:解:当温度降低时,反应①的平衡向正反应方向移动,说明该反应正向为放热反应,△H<0,反应②的平衡向逆反应方向移动,说明该反应正向为吸热反应,△H>0,
已知下列两个气态物质之间的反应:C2H2(g)+H2(g)?C2H4(g)…①,
2CH4(g)?C2H4(g)+2H2(g)…②,
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
(1)C(s)+2H2(g)?CH4(g),△H=-Q1…Ⅰ
(2)C(s)+
H2(g)?
C2H2(g),△H=-Q2…Ⅱ
(3)C(s)+H2(g)?
C2H4(g),△H=-Q3…Ⅲ,
利用盖斯定律,2×[(3)-(2)],得到C2H2(g)+H2(g)?C2H4(g),△H=2(Q2-Q3),
与题干中的①中的方程式一样,而①中的反应为放热反应,则Q2-Q3<0,所以Q2<Q3;
同理:2×[(3)-(1)],得到2CH4(g)?C2H4(g)+2H2(g),△H=2(Q1-Q3),与题干中的②中的方程式一样,而②中的反应为吸热反应,则2(Q1-Q3)>0,所以Q1>Q3;
综上所述Q1>Q3>Q2.
故选:A.
已知下列两个气态物质之间的反应:C2H2(g)+H2(g)?C2H4(g)…①,
2CH4(g)?C2H4(g)+2H2(g)…②,
已知在降低温度时①式平衡向右移动,②式平衡向左移动,则下列三个反应:
(1)C(s)+2H2(g)?CH4(g),△H=-Q1…Ⅰ
(2)C(s)+
| 1 |
| 2 |
| 1 |
| 2 |
(3)C(s)+H2(g)?
| 1 |
| 2 |
利用盖斯定律,2×[(3)-(2)],得到C2H2(g)+H2(g)?C2H4(g),△H=2(Q2-Q3),
与题干中的①中的方程式一样,而①中的反应为放热反应,则Q2-Q3<0,所以Q2<Q3;
同理:2×[(3)-(1)],得到2CH4(g)?C2H4(g)+2H2(g),△H=2(Q1-Q3),与题干中的②中的方程式一样,而②中的反应为吸热反应,则2(Q1-Q3)>0,所以Q1>Q3;
综上所述Q1>Q3>Q2.
故选:A.
点评:本题主要考查了盖斯定律的运用,难度不大,根据所学知识即可完成.

练习册系列答案
相关题目
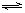 C2H4(g)①
C2H4(g)① 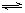 C2H4(g)+2H2(g)②
C2H4(g)+2H2(g)② 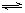 CH4(g);ΔH=-Q1
CH4(g);ΔH=-Q1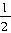 H2(g)
H2(g)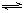
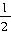 C2H2(g);ΔH=-Q2
C2H2(g);ΔH=-Q2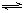
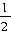 C2H4(g);ΔH=-Q3
C2H4(g);ΔH=-Q3