题目内容
下列说法正确的是( )
A.等物质的量浓度的硫酸氢铵溶液和氢氧化钠溶液等体积混合:c(S042-)>c(Na+)>C(NH4+)>c(OH-)=c(H+)
B.常温下0.4mol/LHB溶液和0.2mol/LNaOH溶液等体积混合后溶液的pH=3,则溶液中微粒浓度存在
下面关系: c(HB)>c(Na+)>c(B-)>c(H+)>c(OH-)
C.在滴有酚酞溶液的氨水中,加入NH4CI的溶液恰好无色,则此时溶液的PH<7
D.pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,若混合液pH=7,则溶液中:2c(R2-)+c(HR-)=c(Na+)
D
【解析】
试题分析:A、等物质的量的硫酸氢铵与氢氧化钠反应,氢氧根离子先与氢离子反应生成硫酸铵、硫酸钠、水,溶液呈酸性,c(S042-)>c(Na+)>C(NH4+)> c(H+)>c(OH-),错误;B、常温下0.4mol/LHB溶液和0.2mol/LNaOH溶液等体积混合后得到的溶液是浓度均为0.1mol/L的NaB和HB混合液,pH=3,溶液呈酸性,说明HB是弱酸且HB电离程度大于B-的水解程度,c(B-)>c(Na+)> c(HB)> c(H+)>c(OH-),错误;C、酚酞的变色范围是8-10,溶液呈无色时,pH<8,错误;D、pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后,若混合液pH=7,溶液呈中性,c(OH-)= c(H+),根据电荷守恒有2c(R2-)+c(HR-)+c(OH-)= c(H+)+ c(Na+),所以有2c(R2-)+c(HR-)=c(Na+),正确,答案选D。
考点:考查溶液混合的判断,离子浓度的大小比较

(16分)2010年8月7日,甘肃甘南藏族自治州舟曲县发生特大泥石流,造成大量人员伤亡,其中饮用水安全在灾后重建中占有极为重要的地位,某研究小组提取三处被污染的水源进行了如下分析:并给出了如下实验信息:其中一处被污染的水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E五种常见化合物都是由下表中的离子形成的:
阳离子 | K+、Na+、Cu2+、Al3+ |
阴离子 | SO |
为了鉴别上述化合物,分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液.
②将E溶液滴入到C溶液中,出现白色沉淀,继续滴加沉淀溶解.
③进行焰色反应,只有B、C为紫色(透过蓝色钴玻璃).
④在各溶液中加入Ba(NO3)2溶液,再加入过量稀硝酸,A中放出无色气体,C、D中产生白色沉淀.
⑤将B、D两溶液混合,未见沉淀或气体生成.
根据上述实验现象填写下列空白:
(1)写出化学式:A 、B________、C 、D________.
(2)将含1 mol A的溶液与含1 mol E的溶液反应后蒸干,仅得到一种化合物,该化合物为________.
(3)写出实验②发生反应的离子方程式______________________________________、
________________________________________________________________________.
(4)C常用作净水剂,用离子方程式表示其净水原理______________________________.

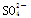 ,那么c(SO42-)应为
,那么c(SO42-)应为

 、HCO
、HCO 、NO
、NO