题目内容
能正确表示下列反应的离子方程式为( )
| A、碘化亚铁溶于稀硝酸中:3Fe2++4H++NO3-=3Fe3++NO↑+2 H2O | ||||
| B、NH4HCO3溶于过量的NaOH溶液中:HCO3-+OH-=CO32-+H2O | ||||
C、向沸水中滴入几滴饱和氯化铁溶液,并加热至溶液成红褐色:Fe3++3H2O
| ||||
| D、大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.漏写碘离子发生的氧化还原反应;
B.漏写铵根离子与碱的反应;
C.水解生成胶体,不是沉淀;
D.反应生成醋酸钙、水、二氧化碳.
B.漏写铵根离子与碱的反应;
C.水解生成胶体,不是沉淀;
D.反应生成醋酸钙、水、二氧化碳.
解答:
解:A.碘化亚铁溶于稀硝酸中的离子反应为Fe2++2I-+4H++NO3-=Fe3++I2+NO↑+2H2O,故A错误;
B.NH4HCO3溶于过量的NaOH溶液中的离子反应为NH4++HCO3-+2OH-=CO32-+H2O+NH3.H2O,故B错误;
C.向沸水中滴入几滴饱和氯化铁溶液,并加热至溶液成红褐色:Fe3++3H2O
Fe(OH)3(胶体)+3H+,故C错误;
D.大理石溶于醋酸中的离子反应为CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O,故D正确;
故选D.
B.NH4HCO3溶于过量的NaOH溶液中的离子反应为NH4++HCO3-+2OH-=CO32-+H2O+NH3.H2O,故B错误;
C.向沸水中滴入几滴饱和氯化铁溶液,并加热至溶液成红褐色:Fe3++3H2O
| ||
D.大理石溶于醋酸中的离子反应为CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O,故D正确;
故选D.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、与量有关的离子反应、水解反应的离子反应考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、在pH=1的溶液中:K+、Na+、SO42-、HCO3- | ||
B、在
| ||
| C、在0.1 mol?L-1 FeCl3溶液中:K+、NH4+、I-、SCN- | ||
| D、在0.1 mol?L-1 Na2CO3溶液中:Al3+、K+、NO3-、SO42- |
下列各组物质均属于硅酸盐制品的是( )
| A、陶瓷、水泥 |
| B、单晶硅、玻璃 |
| C、石膏、漂白粉 |
| D、水玻璃、铝热剂 |
用标准的NaOH溶液滴定未知浓度的盐酸,选用酚酞作指示剂,可导致被测定的盐酸浓度偏高的是( )
| A、未用标准液润洗用蒸馏水洗过的碱式滴定管 |
| B、达到滴定终点,读数时俯视滴定管的刻度 |
| C、滴定过程中振荡锥形瓶有少许盐酸溅出 |
| D、盛装待测液的锥形瓶用蒸馏水洗过,未用待测液润洗 |
下列有关水资源保护的说法中,不正确的是( )
| A、重金属离子对人体有毒,常采用沉淀反应将之除去 |
| B、化肥中含有植物营养素,可大量使用以改善水环境 |
| C、轧钢厂排出的含盐酸的废水,可用熟石灰中和处理 |
| D、天然水中的细小悬浮颗粒,可用明矾等混凝剂净化 |
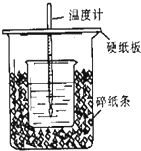 用50mL0.5mol/L的盐酸与50mL0.55mol/L的氢氧化钠在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.5mol/L的盐酸与50mL0.55mol/L的氢氧化钠在如图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 利用如图所示装置制备氧气并进行相关实验探究.
利用如图所示装置制备氧气并进行相关实验探究.