题目内容
19.密度为0.910g/cm3的氨水,质量分数为25.0%,该氨水用等体积的水稀释后,所得溶液的质量分数为( )| A. | 等于12.5% | B. | 大于12.5% | C. | 小于12.5% | D. | 无法确定 |
分析 设浓氨水的体积为V,稀释前后溶液中溶质的质量不变,氨水的密度小于水的密度,浓度越大密度越小,稀释后得到氨水的密度应大于0.91g•cm-3,据此进行解答.
解答 解:设浓氨水的体积为V,密度为ρ浓,稀释后密度为ρ稀,稀释前后溶液中溶质的质量不变,则:稀释后质量分数ω=$\frac{{ρ}_{浓}×V×25%}{2V{ρ}_{稀}}$,
氨水的密度小于水的密度,浓度越大密度越小,所以ρ浓<ρ稀,所以=$\frac{{ρ}_{浓}×V×25%}{2V{ρ}_{稀}}$<12.5%,
故选:C.
点评 本题考查了溶液稀释后质量分数计算,题目难度中等,明确氨水密度小于水、稀释前后溶质的质量不变是解题关键,试题培养了学生的化学计算能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
10.中学化学中的常见物质甲、乙、丙、丁存在如图所示转化关系(反应条件省略),下列说法正确的是( )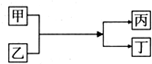

| A. | 若甲为铜,丁为氯化亚铁,则乙一定是氯化铁 | |
| B. | 若甲为水,丁为氢氧化钠,则丙一定是氢气 | |
| C. | 若甲为铝,丁为铁,则乙一定是氧化铁 | |
| D. | 若甲为镁,丁为氢气.则乙一定是酸 |
14. 锰的化合物是优良的催化剂,可用于干电池原料生产等.
锰的化合物是优良的催化剂,可用于干电池原料生产等.
(1)锌锰干电池的反应为2MnO2+Zn+2NH4Cl=2MnO(OH)+Zn(NH3)2Cl2,MnO(OH)中锰元素的化合价为+3.
(2)向废电池还原后的废液(含有Mn2+、Fe2+、Zn2+等)中逐滴滴加Na2S溶液,最先生成的沉淀为ZnS(填化学式).[已知Ksp(MnS)=1.4×10-15,Ksp(ZnS)=2.9×10 -25,Ksp(FeS)=6.0×10-18]
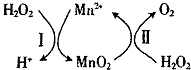
(3)Mn2+催化H2O2分解:2H2O2(l)=2H2O(l)+O2(g)△H1,其反应机理如图:
①已知反应Ⅱ为MnO2(s)+H2O2(1)+2H+ ( aq)=Mn2+ (aq)+O2(g)+2H2O(1)△H2.写出反应 I的热化学方程式(焓变用△H1和△H2表示):H2O2(1)+Mn2+(aq)=2H+(aq)+MnO2(s)△H=△H1-△H2.
②某温度时,向10mL0.4mol/L H2O2液中滴入1滴MnSO4发生分解:2H2O2=2H2O+O2,测得不同时刻生成O2的体积(已折算为标准状况下的体积)如表:
0~2min时反应速率比2~4min时的快,其原因是随着反应的进行,H2O2浓度不断减小,反应速率不断减慢,0~6min的平均反应速率v(H2O2)=3.3×10-2mol/(L•min)(忽略溶液体积的变化).
(4)锰基催化剂是合成甲醇、二甲醚的催化剂.已知:
①反应I的正反应是放热(填“放热”或“吸热”)反应.
②反应Ⅱ的平衡常数表达式为K=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$.
 锰的化合物是优良的催化剂,可用于干电池原料生产等.
锰的化合物是优良的催化剂,可用于干电池原料生产等.(1)锌锰干电池的反应为2MnO2+Zn+2NH4Cl=2MnO(OH)+Zn(NH3)2Cl2,MnO(OH)中锰元素的化合价为+3.
(2)向废电池还原后的废液(含有Mn2+、Fe2+、Zn2+等)中逐滴滴加Na2S溶液,最先生成的沉淀为ZnS(填化学式).[已知Ksp(MnS)=1.4×10-15,Ksp(ZnS)=2.9×10 -25,Ksp(FeS)=6.0×10-18]
(3)Mn2+催化H2O2分解:2H2O2(l)=2H2O(l)+O2(g)△H1,其反应机理如图:
①已知反应Ⅱ为MnO2(s)+H2O2(1)+2H+ ( aq)=Mn2+ (aq)+O2(g)+2H2O(1)△H2.写出反应 I的热化学方程式(焓变用△H1和△H2表示):H2O2(1)+Mn2+(aq)=2H+(aq)+MnO2(s)△H=△H1-△H2.
②某温度时,向10mL0.4mol/L H2O2液中滴入1滴MnSO4发生分解:2H2O2=2H2O+O2,测得不同时刻生成O2的体积(已折算为标准状况下的体积)如表:
| t/min | 0 | 2 | 4 | 6 |
| V(O2)mL | 0 | 9.9 | 17.2 | 22.4 |
(4)锰基催化剂是合成甲醇、二甲醚的催化剂.已知:
| 反应 | 平衡常数KP | |
| 773K | 873K | |
| Ⅰ.CO2(g)+4H2(g)?CH4(g)+2H2(g) | 19.4 | 0.803 |
| Ⅱ.CO2(g)+3H2(g)?CH3OH(g)+H2O(g) | 6.07×10-9 | 3.65×10-9 |
②反应Ⅱ的平衡常数表达式为K=$\frac{c(C{H}_{3}OH)×c({H}_{2}O)}{c(C{O}_{2})×{c}^{3}({H}_{2})}$.
4.用NA表示阿伏德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4L H2O含有的分子数为 NA | |
| B. | 通常状况下,NA 个CO2分子占有的体积为22.4L | |
| C. | 将等物质的量的SO3和SO2溶于水,所得溶液中H+数目相等 | |
| D. | 常温常压下,1.06g Na2CO3溶于水形成的溶液中含有Na+离子数为0.02 NA |
11.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | pH=3的溶液中:K+、Ba2+、Cl-、Br- | |
| B. | 含有0.1mol•L-1Fe3+的溶液中:K+、Mg2+、I-、SO42- | |
| C. | 含有0.1mol•L-1NO3-的溶液中:Na+、H+、SO42-、Fe2+ | |
| D. | 含有大量AlO2-的溶液中:NH4+、NO3-、Cl-、H+ |
8.0.1mol/L的KOH与等浓度等体积的草酸(H2C2O4)溶液混合后,溶液呈酸性,则下列的说法正确的是( )
| A. | 溶液呈酸性说明草酸是弱酸 | B. | c(K+)+c(H+)═c(HC2O4-)+c(OH-)+2c(C2O42-) | ||
| C. | c(K+)>c(HC2O4-)>c(C2O42-)>c(H+) | D. | c(H2C2O4)>c(C2O42-) |
9.下列叙述Ⅰ和Ⅱ均正确并有因果关系的是( )叙述Ⅱ
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 1-已醇的沸点比已烷的沸点高89℃ | 1-已醇和已烷可通过蒸馏初步分离 |
| B | 原电池可将化学能转化为电能 | 原电池需外接电源才能工作 |
| C | H2SO4是离子化合物 | 硫酸溶液可导电 |
| D | 乙二酸可与KMnO4溶液发生反应 | 乙二酸具有酸性 |
| A. | A | B. | B | C. | C | D. | D |