题目内容
16.X、Y、Z为短周期元素,电子层数相同,原子序数依次增大,三种元素的最高价氧化物对应的水化物两两之间均可发生反应.下列说法中正确的是( )| A. | 原子半径:Z>Y>X | |
| B. | X的最高价氧化物对应的水化物中只含有共价键 | |
| C. | X、Z形成的化合物一定为离子化合物 | |
| D. | 工业上常用Y的氯化物为原料制取单质Y |
分析 X、Y、Z为短周期元素,电子层数相同,原子序数依次增大,三种元素的最高价氧化物对应的水化物两两之间均可发生反应,氢氧化铝具有两性,与强碱、强酸反应生成盐和水,则Y为Al,X为Na,Z为S或Cl,以此来解答.
解答 解:由上述分析可知,X为Na,Y为Al,Z为S或Cl,
A.同周期从左向右原子半径减小,则原子半径:X>Y>Z,故A错误;
B.X的最高价氧化物对应的水化物为NaOH,含离子键、共价键,故B错误;
C.X、Z形成的化合物为氯化钠或硫化钠,含离子键,一定为离子化合物,故C正确;
D.Y的氯化物为氯化铝,为共价化合物,不能冶炼Al,故D错误;
故选C.
点评 本题考查原子结构与元素周期律,为高频考点,把握元素的位置、元素化合物知识推断元素为解答的关键,侧重分析与应用能力的考查,注意氢氧化铝具有两性,题目难度不大.

练习册系列答案
相关题目
6.(1)某学习小组通过实验研究Na2O2与水的反应.
①Na2O2的电子式为 ,它与水反应的离子方程式是2Na2O2+2H2O=4Na++4OH-+O2↑.
,它与水反应的离子方程式是2Na2O2+2H2O=4Na++4OH-+O2↑.
②甲同学认为ⅱ中溶液褪色是溶液a中存在较多的H2O2,H2O2与酚酞发生了反应,并实验证实了H2O2的存在:取少量溶液a,加入试剂MnO2(填化学式),有气体产生.
(2)有一瓶澄清的溶液,可有含有大量的NO3-、Fe3+、NH4+、H+、K+、Mg2+、Al3+、SO42-、Ba2+、CO32-、Cl-、I-,现进行如下实验:
①测知溶液显酸性;
②取样加少量四氯化碳和数滴新制氯水,四氯化碳层溶液呈紫红色;
③另取样滴加稀NaOH溶液,使深液变为碱性,此过程中无沉淀生成;
④取少量上述碱性溶液,加Na2CO3溶液出现白色沉淀;
⑤将实验③中的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝.
由此可以推断:
溶液中肯定存在的离子有H+、NH4+、Ba2+、I-.溶液中不能确定是否存在的离子有K+、Cl-.
| 操作 | 现象 |
| 向盛有4.0g Na2O2的烧杯中加入50mL蒸馏水 | 剧烈反应,产生能使带火星木条复燃的气体,得到的无色溶液a |
| 向溶液a中滴入两滴酚酞 | ⅰ.溶液变红 ⅱ.10分种后溶液颜色明显变浅,稍后,溶液变为无色 |
 ,它与水反应的离子方程式是2Na2O2+2H2O=4Na++4OH-+O2↑.
,它与水反应的离子方程式是2Na2O2+2H2O=4Na++4OH-+O2↑.②甲同学认为ⅱ中溶液褪色是溶液a中存在较多的H2O2,H2O2与酚酞发生了反应,并实验证实了H2O2的存在:取少量溶液a,加入试剂MnO2(填化学式),有气体产生.
(2)有一瓶澄清的溶液,可有含有大量的NO3-、Fe3+、NH4+、H+、K+、Mg2+、Al3+、SO42-、Ba2+、CO32-、Cl-、I-,现进行如下实验:
①测知溶液显酸性;
②取样加少量四氯化碳和数滴新制氯水,四氯化碳层溶液呈紫红色;
③另取样滴加稀NaOH溶液,使深液变为碱性,此过程中无沉淀生成;
④取少量上述碱性溶液,加Na2CO3溶液出现白色沉淀;
⑤将实验③中的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝.
由此可以推断:
溶液中肯定存在的离子有H+、NH4+、Ba2+、I-.溶液中不能确定是否存在的离子有K+、Cl-.
7.下列关于有机化合物的说法正确的是( )
| A. | CH2═CHCH(CH3)2的名称是3-甲基-1-丁烯 | |
| B. | 由乙醇生成乙醛属于还原反应 | |
| C. | 乙烯与苯乙烯为同系物 | |
| D. | 乙苯分子中所有碳原子一定共平面 |
4.ClO2是一种消毒杀菌效率高、二次污染小的水处理剂,实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$ClO2↑+K2SO4+2CO2↑+2H2O.下列说法正确的是( )
| A. | lmolKClO3参加反应生成气体的体积为22.4L(标况下) | |
| B. | 该反应的还原产物为CO2 | |
| C. | 0.5mol H2C2O4参加反应有lmol电子转移 | |
| D. | H2SO4在反应中是氧化剂 |
11.短周期元素X、Y、Z、W的原子序数依次增大,X在元素周期表中原子半径最小,Y的次外层电子数是最外层的$\frac{1}{3}$,ZX是一种生氢剂,W与Y同一主族,下列叙述正确的是( )
| A. | 原子半径:rW>rZ>rY | |
| B. | 化合物ZX中各原子均满足8电子稳定结构 | |
| C. | 由X、Y、Z、W组成的化合物的水溶液可能显酸性 | |
| D. | 简单气态氢化物稳定性:W>Y |
8.用NA表示阿伏伽德罗常数的值,下列有关说法正确的是( )
| A. | 标准状况下,33.6LHF中含有氟原子的数目为1.5NA | |
| B. | 1.0L 1.0mol•L-1Na2SO4水溶液中含有的氧原子数为4NA | |
| C. | 电解饱和食盐水,当阴极产生1.12LH2时,转移的电子数为0.1NA | |
| D. | 常温下,2L0.1mol•L-1FeCl3溶液与1L0.2mol•L-1FeCl3溶液所含Fe3+数目不同 |
5.下列说法正确的是( )
| A. | 石蜡油经分馏可以获得乙烯 | |
| B. | 乙二酸、苯酚、苯乙烯均可发生聚合反应 | |
| C. | 室温下,在水中的溶解度:丙烷>乙醇>乙二醇 | |
| D. | 可用碘水和银氨溶液鉴别葡萄糖、麦芽糖和淀粉三种物质 |
6.能正确表示下列反应的离子方程式是( )
| A. | 用石墨作电极电解CuCl2溶液:2Cl-+2H2O$\stackrel{电解}{→}$2OH-+Cl2↑+H2↑ | |
| B. | 0.01mol/LNH4Al(SO4)2溶液与0.02mol/LBa(OH)2溶液等体积混合:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | |
| C. | 将少量二氧化硫通入次氯酸钠溶液:SO2+ClO-+2OH-═SO42-+Cl-+H2O | |
| D. | Ca(HCO3)2溶液与过量NaOH溶液反应:Ca2++HCO3-+OH-═CaCO3+H2O |
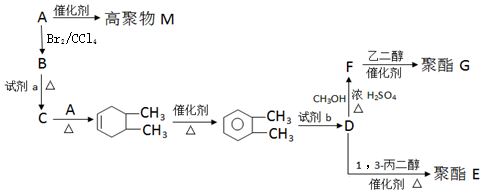
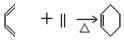
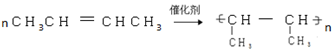 ②B→C
②B→C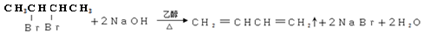
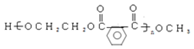 .
. 以CH3CHO为初始原料,选择必要试剂,经过三步反应合成化合物C,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
以CH3CHO为初始原料,选择必要试剂,经过三步反应合成化合物C,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)