题目内容
设NA表示阿伏加德罗常数,下列说法正确的是( )
| A、1 mol氦气中有2NA个氦原子 |
| B、使用摩尔时必须指明粒子的名称 |
| C、1 mol任何物质所含的原子数为NA个 |
| D、1 mol任何物质所含的粒子数为NA个 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、氦气是单原子分子;
B、物质的量是描述微观粒子的物理量,单位为mol;
C、物质的构成可以是原子构成,也可以是分子构成,也可以是离子构成;
D、将NA个微粒看做一个整体,称为1mol.
B、物质的量是描述微观粒子的物理量,单位为mol;
C、物质的构成可以是原子构成,也可以是分子构成,也可以是离子构成;
D、将NA个微粒看做一个整体,称为1mol.
解答:
解:A、氦气是单原子分子,故1mol氦气中含1mol原子,故A错误;
B、物质的量是描述微观粒子的物理量,单位为mol,使用物质的量需要指明微粒种类,故B正确;
C、物质的构成可以是原子构成,也可以是分子构成,也可以是离子构成,1 mol任何物质都含有约6.02×1023个微粒,故C错误;
D、将NA个微粒看做一个整体,称为1mol,故1mol任何物质中含有NA个微粒,故D正确.
故选BD.
B、物质的量是描述微观粒子的物理量,单位为mol,使用物质的量需要指明微粒种类,故B正确;
C、物质的构成可以是原子构成,也可以是分子构成,也可以是离子构成,1 mol任何物质都含有约6.02×1023个微粒,故C错误;
D、将NA个微粒看做一个整体,称为1mol,故1mol任何物质中含有NA个微粒,故D正确.
故选BD.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
下列说法中错误的是( )
| A、氨是一种易溶、易液化的气体 |
| B、氨的水溶液能使紫色石蕊试液变红色 |
| C、氨气不能用浓硫酸来干燥 |
| D、氨气在一定条件下能跟氧气反应 |
将铜和锌用导线连接插入硫酸铜溶液中,当导线中有0.2mol电子通过时,负极质量变化是( )
| A、增加6.5g |
| B、减少6.5g |
| C、减少5.6g |
| D、增加5.6g |
下列属于纯净物的是( )
| A、液氨 | B、浓氨水 |
| C、纯盐酸 | D、65%的硝酸 |
在标准状况下,将22.4L HCl气体溶于水制成0.5L盐酸,所得盐酸的物质的量浓度为( )
| A、2mol/L |
| B、1.2mol/L |
| C、0.8mol/L |
| D、无法计算 |
设NA为阿伏加德罗常数的值,下列叙述不正确的( )
| A、10g质量分数为46%的乙醇溶液中,氢原子的总数为1.2NA |
| B、5.6 g铁与足量硫加热充分反应转移电子数为 0.2NA |
| C、50 mL 12 mol?L-1 浓盐酸与足量二氧化锰加热反应,转移电子数为0.3 NA |
| D、标准状况下,含有1mol硫原子的SO2与SO3的混合物,其体积小于22.4L |
下列说法正确的是 ( )
| A、标况下,1mol任何物质的体积都约为22.4L |
| B、1mol气体的体积约为22.4L |
| C、标况下,1molO2和N2混合气(任意比)的体积约为22.4L |
| D、22.4L气体所含分子数一定大于11.2L气体所含的分子数 |
 北京大学和中国科学院的化学工作者合作,已成功研制出碱金属与C60形成的石墨夹层离子化合物.将石墨置于熔融的钾或气态的钾中,石墨吸收钾而形成称为钾石墨的物质,其组成可以是C8K、C12K、C24K、C36K、C48K、C60K等等.在钾石墨中,钾原子把价电子交给石墨层,但在遇到与金属钾易反应的其他物质时还会收回.下列分析中正确的是( )
北京大学和中国科学院的化学工作者合作,已成功研制出碱金属与C60形成的石墨夹层离子化合物.将石墨置于熔融的钾或气态的钾中,石墨吸收钾而形成称为钾石墨的物质,其组成可以是C8K、C12K、C24K、C36K、C48K、C60K等等.在钾石墨中,钾原子把价电子交给石墨层,但在遇到与金属钾易反应的其他物质时还会收回.下列分析中正确的是( )| A、题干中所举出的6种钾石墨,属于同素异形体 | ||
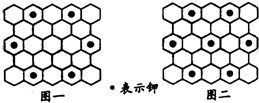
| B、若某钾石墨的原于分布如图一所示,则它所表示的是C24K | ||
| C、若某钾石墨的原子分布如图二所示,则它所表示的是C12K | ||
D、另有一种灰色的钾石墨C32K,其中K的分布也类似图中的中心六边形,则最近两个K原子之间的距离为石墨键长的4
|