题目内容
4.对于常温下pH=12的氨水,下列说法正确的是( )| A. | 向溶液中加入稀盐酸可以促进氨水的电离,溶液的碱性增强 | |
| B. | 向溶液中加入等体积的pH=2盐酸后溶液呈酸性 | |
| C. | 由水电离产生的c(OH-)=10-12mol•L-1 | |
| D. | 向溶液中加入适量盐酸使混合液的pH=7,混合液中c(NH4+)>c(Cl-) |
分析 A、向溶液中加入稀盐酸可以促进氨水的电离,但溶液的酸性增强,碱性减弱;
B、加入等体积的pH=2盐酸得到氯化铵和一水合氨的混合物;
C、由水电离产生的c(OH-)=c(H+);
D、pH=7,则c(OH-)=c(H+),根据电荷守恒判断c(NH4+)、c(Cl-).
解答 解:A、向溶液中加入稀盐酸可以促进氨水的电离,但溶液的酸性增强,碱性减弱,故A错误;
B、加入等体积的pH=2盐酸得到氯化铵和一水合氨的混合物,以一水合氨的电离为主,溶液呈碱性,故B错误;
C、由水电离产生的c(OH-)=c(H+)=10-12mol•L-1,故C正确;
D、pH=7,则c(OH-)=c(H+),根据电荷守恒得c(NH4+)=c(Cl-),故D错误;
故选C.
点评 本题考查弱电解质的电离,明确弱电解质电离特点是解本题关键,会计算酸中水电离氢离子浓度、碱中水电离氢氧根离子浓度,为易错点.

练习册系列答案
相关题目
14.ClO2是一种消毒杀菌效率高,二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4═2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法正确的是( )
| A. | 1mol KClO3参加反应有2mol电子转移 | |
| B. | H2C2O4在反应中被还原 | |
| C. | 还原性:H2C2O4>ClO2 | |
| D. | ClO2是氧化产物 |
15.深海中存在可燃冰(CH4•nH2O固体).已知:CH4•nH2O(s)?CH4(g)+nH2O(l)-Q(Q>0)深海中能够存在可燃冰,是因为深海具有以下条件中的( )
| A. | 低温高压 | B. | 高温低压 | C. | 低温低压 | D. | 高温高压 |
12.对于方程式2H2S+O2→2S+2H2O和2H2S+SO2→3S↓+2H2O,所得结论中,正确的是( )
| A. | 化合价升降总数不等 | B. | 这两个反应的类型不相同 | ||
| C. | 产物种类相同 | D. | 硫元素价态变化相同 |
9.根据如图转化关系判断下列说法不正确的是( )
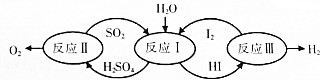

| A. | 反应Ⅰ中SO2是还原剂 | B. | 反应Ⅲ中H2是还原产物 | ||
| C. | 氧化性强弱顺序:H2SO4>I2>SO2 | D. | 该转化关系可实现分解H2O制取H2 |
1.下列各组比较不正确的是( )
| A. | 金属性强弱:Na>Mg>Al | B. | 热稳定性:HCl>H2 S>PH3 | ||
| C. | 酸性强弱:HClO4>H2 SO4>H3PO4 | D. | 熔点:Na>SiO2>CO2 |
2.下列离子在无色溶液中大量共存的是( )
| A. | Fe3+、Na+、SCN-、Cl- | B. | Na+、H+、NO3-、SO42- | ||
| C. | Na+、OH-、H+、NO3- | D. | Fe2+、NH4+、Cl-、OH- |