题目内容
7.氨是最重要的氮肥,是产量最大的化工产品之一.德国人哈伯在1905年发明了合成氨的方法,其合成原理为:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1,他因此获得了1918年诺贝尔化学奖. 在密闭容器中,使2mol N2和6mol H2混合发生下列反应:N2(g)+3H2(g)?2NH3(g)(正反应为放热反应)(1)当反应达到平衡时,N2和H2的转化率比是1:1.
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量变小,
密度不变.(填“变大”“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将逆向(填“正向”“逆向”或“不”)移动.
分析 (1)加入的氮气和氢气的物质的量之比等于其化学计量数之比,无论反应到什么程度,氮气和氢气的转化率之比始终相等;
(2)平均相对分子质量=$\frac{气体总质量}{气体总物质的量}$,ρ=$\frac{m}{V}$,据此进行计算;
(3)充入氩气并保持压强不变,体积变大,各组分浓度减小.
解答 解:(1)加入的氮气和氢气的物质的量之比等于其化学计量数之比,无论反应到什么程度,用氮气和氢气表示的速率正比等于化学计量数之比,所以氮气和氢气的转化率之比为1:1,
故答案为:1:1;
(2)升温,平衡逆向移动,气体物质的量增大,质量不变,气体的平均相对分子质量=$\frac{气体总质量}{气体总物质的量}$,所以混合气体的平均相对分子质量减小;
因容器体积不变,气体总质量不变,所以混合气体的密度不变,
故答案为:变小;不变;
(3)充入氩气并保持压强不变,体积变大,相关气体的分压变小,相当于减小压强,平衡向体积增大的逆向移动,
故答案为:逆向.
点评 本题考查了化学平衡的计算,题目难度中等,明确化学平衡及其影响为解答关键,注意掌握化学反应速率、平均相对分子质量的概念及表达式,试题培养了学生的分析能力及化学计算能力.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
9.下列关于甲烷与Cl2的取代反应所得产物的说法正确的是( )
| A. | 都是有机物 | B. | 都不溶于水 | ||
| C. | 有一种气态物质,其余均是液体 | D. | 除一种外均是四面体结构 |
19.用适量水稀释0.1mol/L氨水时,溶液中随着水量的增加而减小的是( )
| A. | c(OH-) | B. | n(NH4+) | C. | $\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$ | D. | n(OH-) |
16.下列对应关系或事实的解释正确的是( )
| A. | NH4Cl水解呈酸性,不能用来当做肥料使用 | |
| B. | 氧化镁的熔点高,可用于制作耐高温的材料 | |
| C. | 氯碱工业中的“碱”指的是Na2CO3 | |
| D. | 水泥、玻璃等硅酸盐材料指的是以二氧化硅为原料生产的材料 |
17.在一定温度下,向2L密闭容器中加入1mol X和2mol Y,发生如下反应:X(g)+2Y(g)?2Z(g),此反应达到平衡的标志是( )
| A. | 容器内气体混合物的密度不随时间变化 | |
| B. | 容器内X、Y、Z浓度之比为1:2:2 | |
| C. | 容器内气体混合物的压强不随时间变化 | |
| D. | 单位时间内消耗0.1mol X,同时生成0.2mol Z |
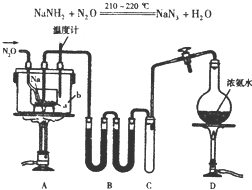 NaN3(叠氮化钠)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂.实验室制取叠氮化钠的原理、实验装置及步骤如下:
NaN3(叠氮化钠)是一种易溶于水的白色晶体,微溶于乙醇,不溶于乙醚,常用作汽车安全气囊中的药剂.实验室制取叠氮化钠的原理、实验装置及步骤如下: