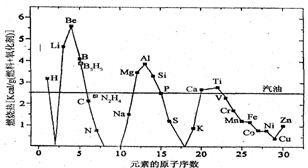
题目内容
运用相关化学知识进行判断,下列结论错误的是( )
| A、增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率 |
| B、NH4F水溶液中含有HF,因此NH4F溶液不能存放于玻璃试剂瓶中 |
| C、可燃冰主要甲烷与水在低温高压下形成的水合物晶体,因此可存在于海底 |
| D、需要加热的反应不一定是吸热反应 |
考点:化学反应速率的影响因素,反应热和焓变,盐类水解的应用
专题:基本概念与基本理论
分析:A.浓硫酸与铁发生反应生成二氧化硫气体;
B.HF与二氧化硅反应;
C.海底温度较低,压强较大,适合形成甲烷的水合物晶体;
D.反应是否加热才能进行,与吸热、放热反应无关.
B.HF与二氧化硅反应;
C.海底温度较低,压强较大,适合形成甲烷的水合物晶体;
D.反应是否加热才能进行,与吸热、放热反应无关.
解答:
解:A.浓硫酸与铁发生氧化还原反应生成二氧化硫,故A错误;
B.HF与二氧化硅反应而腐蚀玻璃,不能存放于玻璃试剂瓶中,故B正确;
C.海底温度较低,压强较大,适合形成甲烷的水合物晶体,故C正确;
D.反应是否加热才能进行,与吸热、放热反应无关,如铝热反应为放热反应,在需在加热条件下进行,故D正确.
故选A.
B.HF与二氧化硅反应而腐蚀玻璃,不能存放于玻璃试剂瓶中,故B正确;
C.海底温度较低,压强较大,适合形成甲烷的水合物晶体,故C正确;
D.反应是否加热才能进行,与吸热、放热反应无关,如铝热反应为放热反应,在需在加热条件下进行,故D正确.
故选A.
点评:本题考查较为综合,涉及浓硫酸、氢氟酸、甲烷以及化学反应与能力变化等知识,为高考常见题型,侧重于学生的分析能力和双基的考查,难度中等,注意相关基础知识的积累.

练习册系列答案
相关题目
固体碘在受热时发生升华现象,有关叙述正确的是( )
| A、碘受热升华,破坏的是分子间作用力,未破坏I-I共价键,因此未发生吸热反应 |
| B、碘受热升华,吸收热量,发生了吸热反应 |
| C、碘升华,未破坏共价键,不供应热量也能发生 |
| D、碘升华过程中,热能转变为化学能 |
次磷酸钠(NaH2PO2)是唯一的次磷酸的钠盐(不存在酸式盐).下列叙述中正确的是( )
| A、次磷酸(H3PO2)是三元酸 |
| B、H3PO2中磷为+1价 |
| C、NaH2PO2溶液呈酸性 |
| D、次磷酸根离子为-3价 |
水热法制备Fe3O4纳米颗粒的化学方程式为:3Fe++2S2O
+O2+4OH-=Fe3O4+X+2H2O.下列有关说法不正确的是( )
2- 3 |
| A、上式中的X为S4O62- |
| B、该反应中的还原剂为Fe2+和S2O32- |
| C、当生成1 mol Fe3O4时,转移电子的物质的量为4 mol |
| D、当3 mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1 mol |
X和Y均为短周期元素,已知aXn-比bYm+多两个电子层,则下列说法正确的是( )
| A、b<5 |
| B、X只能位于第三周期 |
| C、a+n-b+m=10或16 |
| D、Y不可能位于第二周期 |
S-诱抗素的分子结构如图所示,下列关于该物质的说法正确的是( )
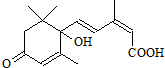

| A、其分子式为C15H22O4 |
| B、1mol该物质与NaOH溶液反应,最多消耗2mol NaOH |
| C、能发生加聚反应 |
| D、不能使酸性KMnO4溶液褪色 |
根据原子结构及元素周期律的知识,下列推断正确的是( )
| A、同主族元素含氧酸的酸性随核电荷数的增加而减弱 | ||||
| B、核外电子排布相同的微粒化学性质也相同 | ||||
| C、S2?、Cl?、K+、Ca2+半径逐渐减小 | ||||
D、
|