题目内容
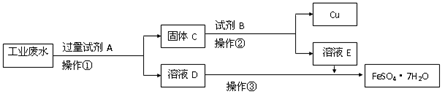 某工厂的酸性废水中含有大量的Fe3+、Cu2+、SO42-和少量Na+.为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾.
某工厂的酸性废水中含有大量的Fe3+、Cu2+、SO42-和少量Na+.为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾.(1)工业废水中加入试剂A后,反应的离子方程式为Fe+Cu2+═Fe2++Cu、Fe+2H+═Fe2++H2↑、
(2)试剂B是
(3)操作③是蒸发浓缩、冷却结晶、
(4)可用绿矾消除工业废水中+6价铬(Cr2O72-)的污染,使之转化为Cr3+,若处理1t废水(含Cr2O72- 10-3mol/kg),则需加入绿矾的质量至少为
考点:物质分离和提纯的方法和基本操作综合应用
专题:实验设计题
分析:某工厂的工业废水中含有大量的Fe3+、Cu2+、SO42-和少量Na+,先加过量铁(A),过滤,得到D溶液为FeSO4,C为Cu和多余的铁,再向C中加过量稀硫酸,过滤得到的Cu,E为FeSO4,硫酸亚铁经过蒸发浓缩、冷却结晶可以得到绿矾晶体,
(1)根据能和金属铁发生反应的物质来回答;
(2)试剂B是将金属铜和金属铁分离开的物质;
(3)从FeSO4溶液中提取溶质晶体采用蒸发结晶;
(4)亚铁离子变质会生成铁离子,(Cr2O72-)转化为Cr3+,根据电子守恒得到二者之间的关系式,进行计算即可.
(1)根据能和金属铁发生反应的物质来回答;
(2)试剂B是将金属铜和金属铁分离开的物质;
(3)从FeSO4溶液中提取溶质晶体采用蒸发结晶;
(4)亚铁离子变质会生成铁离子,(Cr2O72-)转化为Cr3+,根据电子守恒得到二者之间的关系式,进行计算即可.
解答:
解:工厂的工业废水中含有大量的Fe3+、Cu2+、SO42-和少量Na+,先加过量铁(A),过滤,得到D溶液为FeSO4,C为Cu和多余的铁,再向C中加过量稀硫酸,过滤得到的Cu,E为FeSO4,硫酸亚铁经过蒸发浓缩、冷却结晶可以得到绿矾晶体,
(1)酸性环境Fe3+、Cu2+、SO42-和少量Na+中,能和金属铁发生反应的物质是Fe3+、Cu2+、H+,发生的反应有:Fe+Cu2+═Fe2++Cu、Fe+2H+═Fe2++H2↑、2Fe3++Fe═3Fe2+,故答案为:2Fe3++Fe═3Fe2+;
(2)试剂B是将金属铜和金属铁分离开的物质,可以选择稀硫酸,故答案为:H2SO4(硫酸);
(3)从FeSO4溶液中提取溶质晶体采用蒸发浓缩、冷却结晶、过滤,最后用少量冷水洗涤晶体,在低温下干燥,防止变质,故答案为:过滤;
(4)亚铁离子变质会生成铁离子,(Cr2O72-)转化为Cr3+,根据电子守恒得到二者之间的关系式:Cr2O72-~6Fe2+,
Cr2O72-~6Fe2+
1 6
1000kg×10-3mol/kg 6mol
处理1t废水(含Cr2O72- 10-3mol/kg),则需加入绿矾的质量是6mol×278g/mol=1668g.故答案为:1668g.
(1)酸性环境Fe3+、Cu2+、SO42-和少量Na+中,能和金属铁发生反应的物质是Fe3+、Cu2+、H+,发生的反应有:Fe+Cu2+═Fe2++Cu、Fe+2H+═Fe2++H2↑、2Fe3++Fe═3Fe2+,故答案为:2Fe3++Fe═3Fe2+;
(2)试剂B是将金属铜和金属铁分离开的物质,可以选择稀硫酸,故答案为:H2SO4(硫酸);
(3)从FeSO4溶液中提取溶质晶体采用蒸发浓缩、冷却结晶、过滤,最后用少量冷水洗涤晶体,在低温下干燥,防止变质,故答案为:过滤;
(4)亚铁离子变质会生成铁离子,(Cr2O72-)转化为Cr3+,根据电子守恒得到二者之间的关系式:Cr2O72-~6Fe2+,
Cr2O72-~6Fe2+
1 6
1000kg×10-3mol/kg 6mol
处理1t废水(含Cr2O72- 10-3mol/kg),则需加入绿矾的质量是6mol×278g/mol=1668g.故答案为:1668g.
点评:本题考查了工艺流程图的分析判断,解答本题要充分理解各种物质的性质,从而得出正确的结论,应熟悉混合物的分离方法,掌握过滤和蒸发结晶分离方法的使用条件及实验操作,题目难度中等.

练习册系列答案
相关题目
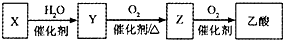 某石油化工产品X的转化关系如图,下列判断正确的是( )
某石油化工产品X的转化关系如图,下列判断正确的是( )| A、X与H2O生成Y的反应是加成反应 |
| B、1 mol Y与足量金属钠反应,能生成3 mol H2 |
| C、Z与CH3OCH3互为同分异构体 |
| D、0.1 mol?L-1乙酸溶液pH为1 |
下列有关官能团的叙述错误的是( )
| A、不同类的有机物可以有相同的官能团 |
| B、醚类的官能团是醚键 |
| C、所有的烷烃和芳香烃都没有官能团 |
| D、同一有机物可以含不同种官能团 |
1mol某烃能与2molHCl完全加成,其产物最多能被6molCl2完全取代,则原烃可能为( )
| A、乙炔 |
| B、1,3-丁二烯 |
| C、1-丙炔 |
| D、1,3-环己二烯 |