题目内容
18.NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 常温常压下,11.2 L氯气所含原子数目为NA | |
| B. | 2 L 0.2 mol/L K2SO4溶液SO42-物质的量浓度为0.4 mol/L | |
| C. | 1 mol Na作还原剂可提供电子数为NA | |
| D. | 同温、同压下NA个CO2分子和NA个O2分子的体积相同 |
分析 A、常温常压下,气体摩尔体积大于22.4L/mol;
B、1mol硫酸钾中含1mol硫酸根;
C、根据反应后钠元素为+1价来分析;
D、同温同压下,二氧化碳和氧气的状态不一定相同.
解答 解:A、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氯气的物质的量小于0.5mol,则原子个数小于NA个,故A错误;
B、1mol硫酸钾中含1mol硫酸根,故0.2mol/L的硫酸钾溶液中硫酸根的浓度为0.2mol/L,故B错误;
C、由于反应后钠元素为+1价,故1mol钠失去1mol电子即NA个,故C正确;
D、同温同压下,二氧化碳和氧气的状态不一定相同,则体积不一定相同,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
8.在0.1mol•L-1NH3•H2O溶液中存在如下电离平衡:NH3•H2O?NH4++OH-.对于该平衡,下列叙述中正确的是( )
| A. | 加入水时,溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| B. | 加入少量NaOH固体,平衡向逆反应方向移动,电离平衡常数减小 | |
| C. | 加入少量0.1 mol•L-1HCl溶液,溶液中c(OH-)增大 | |
| D. | 降低温度,溶液中c(NH4+)增大 |
6. 在10L密闭容器中,A、B、C三种气态物质构成了可逆反应体系;某温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二.下列分析正确的是( )
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应体系;某温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二.下列分析正确的是( )
 在10L密闭容器中,A、B、C三种气态物质构成了可逆反应体系;某温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二.下列分析正确的是( )
在10L密闭容器中,A、B、C三种气态物质构成了可逆反应体系;某温度时,A、B、C物质的量与时间的关系如图一,C的百分含量与温度的关系如图二.下列分析正确的是( )| A. | 0~4 min时,A的平均反应速率为0.1 mol/(L•min) | |
| B. | 该反应是一个吸热反应 | |
| C. | 平衡后升高温度,K值增大 | |
| D. | 该反应的平衡常数表达式为:K=$\frac{c(C)}{{c}^{2}(A)c(B)}$ |
13.磁流体是电子材料的新秀,它既具有固体的磁性,又具有液体的流动性,可用于潜水艇推进器等.制备某种磁流体时,将等物质的量的硫酸亚铁溶液和硫酸铁溶液混合,滴入稍过量的氢氧化钠溶液,随后加入油酸钠溶液,所得磁流体黑色粒子直径在5.5~36nm之间.下列说法正确的是( )
| A. | 所得的分散系属于悬浊液 | B. | 所得的分散系中的分散质为Fe2O3 | ||
| C. | 给分散系通电时阳极周围黑色不变 | D. | 该分散系能产生丁达尔效应 |
3.加入适量的硫酸,可使下列的离子浓度减小的是( )
| A. | Na+ | B. | H+ | C. | CO32- | D. | Cl- |
10.下列操作过程中,利用物质的氧化性的是( )
| A. | 明矾净化水 | B. | 纯碱除去油污 | ||
| C. | 臭氧用于餐具消毒 | D. | 食醋清洗水垢 |
7.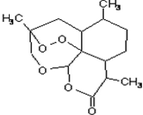 青蒿素是抗恶性疟疾特效药,结构如图所示,下列关于青蒿素的说法正确的是( )
青蒿素是抗恶性疟疾特效药,结构如图所示,下列关于青蒿素的说法正确的是( )
 青蒿素是抗恶性疟疾特效药,结构如图所示,下列关于青蒿素的说法正确的是( )
青蒿素是抗恶性疟疾特效药,结构如图所示,下列关于青蒿素的说法正确的是( )| A. | 分子式是C15H22O5 | |
| B. | 易溶于水,乙醇和乙醚 | |
| C. | 含有-O-O-键,具有较强的氧化性 | |
| D. | 1mol青蒿素可以和1molH2发生加成反应 |
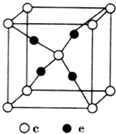 周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子.回答下列问题:
周期表前四周期的元素a、b、c、d、e,原子序数依次增大.a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子.回答下列问题: .
.