题目内容
 某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.
某研究小组用如图所示装置进行铜与浓硫酸反应的实验研究.(1)写出试管B中的实验现象:
(2)B试管口蘸有NaOH溶液的棉花的作用:
(3)向A试管中加入H2O2,发现剩余铜片继续溶解,反应的离子方程式为:
(4)若不补充浓硫酸,只要求使铜片溶解,也可以加入:
(5)将反应产生的气体缓缓通入含有0.1mol Ca(OH)2的澄清石灰水中,充分反应得到0.05mol沉淀,则通入的气体的体积(标准状况)是多少?(请写出解题过程)
考点:浓硫酸的性质实验
专题:实验设计题
分析:(1)二氧化硫具有漂白性;
(2)二氧化硫为有毒气体,不能排放到空气中,二氧化硫为酸性气体,与NaOH溶液反应;
(3)在酸性条件下,过氧化氢具有强氧化性,能氧化Cu而生成铜离子;
(4)铜离子、稀硝酸等也能够溶解铜;
(5)生成的沉淀为亚硫酸钙,若二氧化硫不足,则二氧化硫的物质的量为0.05mol;若二氧化硫过量,则0.1mol氢氧化钙完全反应,其中生成0.05mol亚硫酸钙、0.05mol亚硫酸氢钙,则二氧化硫的物质的量为0.05mol×2+0.05mol=0.15mol,然后根据V=nVm计算出标况下二氧化硫的体积.
(2)二氧化硫为有毒气体,不能排放到空气中,二氧化硫为酸性气体,与NaOH溶液反应;
(3)在酸性条件下,过氧化氢具有强氧化性,能氧化Cu而生成铜离子;
(4)铜离子、稀硝酸等也能够溶解铜;
(5)生成的沉淀为亚硫酸钙,若二氧化硫不足,则二氧化硫的物质的量为0.05mol;若二氧化硫过量,则0.1mol氢氧化钙完全反应,其中生成0.05mol亚硫酸钙、0.05mol亚硫酸氢钙,则二氧化硫的物质的量为0.05mol×2+0.05mol=0.15mol,然后根据V=nVm计算出标况下二氧化硫的体积.
解答:
解:(1)二氧化硫具有漂白性,能使品红褪色,故答案为:品红溶液褪色;
(2)二氧化硫为有毒气体,不能排放到空气中,根据二氧化硫为酸性气体,应用NaOH溶液吸收,
故答案为:吸收二氧化硫,防止污染空气;
(3)在酸性条件下,过氧化氢具有强氧化性,能氧化Cu而生成铜离子和水,反应的方程式为:Cu+H2O2+2H+=Cu2++2H2O,
故答案为:Cu+H2O2+2H+=Cu2++2H2O;
(4)铜离子、稀硝酸也能够溶解铜,也可选用Cu(NO3)2或HNO3,
故答案为:Cu(NO3)2;HNO3;
(5)当二氧化硫不足,反应完全生成亚硫酸钙时,根据S原子守恒可知,二氧化硫的物质的量为0.05mol,标况下体积为:22.4L/mol×0.05mol=1.12L;
当二氧化硫部分过量时,反应生成亚硫酸钙和亚硫酸氢根离子的混合物,其中0.05mol为亚硫酸钙,则亚硫酸氢钙的物质的量为0.05mol,根据S原子守恒可知二氧化硫的物质的量为:0.05mol×2+0.05mol=0.15mol,标况下0.15mol二氧化碳的体积为:22.4L/mol×0.15mol=3.36L,
答:通入的标况下二氧化硫的体积为1.12L或3.36L.
(2)二氧化硫为有毒气体,不能排放到空气中,根据二氧化硫为酸性气体,应用NaOH溶液吸收,
故答案为:吸收二氧化硫,防止污染空气;
(3)在酸性条件下,过氧化氢具有强氧化性,能氧化Cu而生成铜离子和水,反应的方程式为:Cu+H2O2+2H+=Cu2++2H2O,
故答案为:Cu+H2O2+2H+=Cu2++2H2O;
(4)铜离子、稀硝酸也能够溶解铜,也可选用Cu(NO3)2或HNO3,
故答案为:Cu(NO3)2;HNO3;
(5)当二氧化硫不足,反应完全生成亚硫酸钙时,根据S原子守恒可知,二氧化硫的物质的量为0.05mol,标况下体积为:22.4L/mol×0.05mol=1.12L;
当二氧化硫部分过量时,反应生成亚硫酸钙和亚硫酸氢根离子的混合物,其中0.05mol为亚硫酸钙,则亚硫酸氢钙的物质的量为0.05mol,根据S原子守恒可知二氧化硫的物质的量为:0.05mol×2+0.05mol=0.15mol,标况下0.15mol二氧化碳的体积为:22.4L/mol×0.15mol=3.36L,
答:通入的标况下二氧化硫的体积为1.12L或3.36L.
点评:本题考查浓硫酸的化学性质,题目难度中等,注意掌握铜与浓硫酸的反应原理,明确二氧化硫的性质及检验方法、浓硫酸的化学性质,试题培养了学生的分析、理解能力及化学实验能力.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
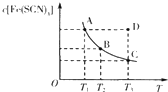 已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )
已知:FeCl3(aq)+3KSCN(aq)?3KCl(aq)+Fe(SCN)3(aq),平衡时Fe(SCN)3的物质的量浓度与温度T的关系如图所示,则下列说法正确的是( )| A、A点与B点相比,A点的c( Fe3+)大 |
| B、加入KCl固体可以使溶液由D点变到C点 |
| C、反应处于D点时,一定有υ(正)<υ(逆) |
| D、若T1、T2温度下的平衡常数分别为K1、K2,则K1<K2 |
下列化学用语的表述正确的是( )
A、离子结构示意图: 可以表示16O2-,也可以表示18O2- 可以表示16O2-,也可以表示18O2- |
B、比例模型: 可以表示甲烷分子,也可以表示四氯化碳分子 可以表示甲烷分子,也可以表示四氯化碳分子 |
C、氯化铵的电子式为: |
| D、CO2的结构式为:O-C-O |
如图为两种途径制备硫酸的过程(反应条件略),下列说法不正确的是( )


| A、途径②增大02浓度可提高SO2转化率 |
| B、含l mol H2S04的浓溶液与足量NaOH反应,放出的热量即为中和热 |
| C、途径②中S02和S03均属于酸性氧化物 |
| D、若△Hl<△H2+△H3,则2H202(aq)=2H20(1)+02 (g)为放热反应 |
下列各组物质中,化学键类型相同,晶体类型也相同的是( )
| A、CH4和 H2O |
| B、KCl 和 HCl |
| C、Cl2 和 KCl |
| D、SiO2 和 CO2 |
只有在化合物中才能存在的化学键是( )
| A、离子键 | B、共价键 |
| C、极性键 | D、非极性键 |
X、Y、Z是原子序数依次增大且属于不同周期的三种常见短周期元素,三种元素相互之间可以形成1:1型的化合物R、M、N,常温下M、N为固体,R为液体.M、N遇到水都能产生气体,而且产生的气体相互可以化合,下列说法正确的是( )
| A、三种元素都是非金属元素 |
| B、由三种元素形成的物质既含离子键又含共价键 |
| C、三种化合物都是共价化合物 |
| D、各1mol的M、N与水反应所得气体体积比为1:1 |
下列离子方程式书写错误的是( )
| A、氯化铝溶液与少量NaOH溶液反应Al3++3OH-=Al(OH)3↓ |
| B、Al(OH)3溶于NaOH溶液中:Al(OH)3+OH-=AlO2-+2H2O |
| C、NaAlO2溶液中通入过量的CO2:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32- |
| D、Al2O3粉末溶于NaOH溶液中:Al2O3+2OH-=2AlO2-+H2O |
某无色溶液中只可能含有Na+、K+、Fe3+、NH4+、Cu2+、SO42-、SO32-、CO32-、Cl-、Br-这几种离子中的若干种,依次进行下列实验,观察到的现象记录如下:
①pH试纸检验,溶液呈碱性;
②取少量原溶液,向溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成.
③另取少量原溶液,向溶液中滴加足量氯水,再加入CCl4振荡,静置后CCl4层呈橙红色.
④向分液后的水溶液中加入Ba(NO3)2溶液和HNO3溶液,有白色沉淀产生,过滤.
⑤在滤液中加入AgNO3和HNO3的混合溶液有白色沉淀产生.则关于原溶液的判断中不正确的是( )
①pH试纸检验,溶液呈碱性;
②取少量原溶液,向溶液中加入过量的BaCl2和盐酸的混合溶液,无白色沉淀生成.
③另取少量原溶液,向溶液中滴加足量氯水,再加入CCl4振荡,静置后CCl4层呈橙红色.
④向分液后的水溶液中加入Ba(NO3)2溶液和HNO3溶液,有白色沉淀产生,过滤.
⑤在滤液中加入AgNO3和HNO3的混合溶液有白色沉淀产生.则关于原溶液的判断中不正确的是( )
| A、肯定不存在的离子是Fe3+、Cu2+、NH4+、SO42-、CO32- |
| B、肯定存在的离子是Na+、K+、CO32-、Br- |
| C、无法确定原溶液中是否存在Cl- |
| D、若步骤④改用BaCl2溶液和盐酸的混合溶液,则对溶液中离子的判断无影响 |