题目内容
12.下列指定微粒的个数比等于2:1的是( )| A. | ${\;}_{1}^{2}$H原子中的中子数和质子数 | |
| B. | ${\;}_{18}^{36}$Ar原子中的质量数与中子数 | |
| C. | ${\;}_{4}^{8}$Be2+中的质子数和电子数 | |
| D. | ${\;}_{12}^{26}$Mg2+中的中子数和电子数 |
分析 元素符号的左上角为质量数、左下角为质子数,原子序数=质子数=核电荷数=核外电子数,质量数=质子数+中子数,阳离子核外电子数=质子数-所带电荷数,阴离子核外电子数=质子数+所带电荷数,据此分析解答.
解答 解:A.${\;}_{1}^{2}$H原子中的质子数为1,质量数为2,中子数=2-1=1,中子数和质子数个数比等于1:1,故A错误;
B.${\;}_{18}^{36}$Ar原子中的质量数为36,中子数为36-18=18,质量数与中子数个数比等于2:1,故B正确;
C.${\;}_{4}^{8}$Be2+中的质子数为4,电子数为4-2=2,质子数和电子数个数比等于4:2=2:1,故C正确;
D.${\;}_{12}^{26}$Mg2+中的中子数为26-12=14,电子数为12-2=10,中子数和电子数个数比等于14:10=7:5,故D错误;
故选BC.
点评 本题原子结构,注意原子中的数量关系即可解答,侧重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
2.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol•L-1 NaOH溶液中Na+的数目为0.1 NA | |
| B. | 标准状况下,2.24 L CCl4中的分子数目为0.1 NA | |
| C. | 0.1 mol Na2O2与足量CO2反应转移的电子数目为0.1 NA | |
| D. | 3.2 g O2和O3的混合物含有的分子数目为0.1 NA |
20.下列有关NaClO和NaCl混合溶液的叙述正确的是( )
| A. | 该溶液中,NH4+、Fe2+、SO42-、Br-可以大量共存 | |
| B. | 该溶液中,K+、Ag+、H+、NO3-可以大量共存 | |
| C. | 向该溶液中通入SO2气体,反应的离子方程式为SO2+3CIO-+H2O═SO42-+CI-+2HCIO | |
| D. | 向该溶液中加入浓盐酸,反应的离子方程式为CIO-+CI-+2H+═Cl2↑+H2O |
17.镁铝合金4.08g溶于250mL2mol/L的盐酸中,标准状况下放出气体的体积为4.48L,向反应后的溶液中加入500mLNaOH溶液,充分反应后最终产生白色沉淀.下列有关说法不正确的是( )
| A. | 4.08g镁铝合金中含有镁和铝的质量分别为1.92g、2.16g | |
| B. | 生成沉淀的最大质量为10.88g | |
| C. | 若白色沉淀只有Mg(OH)2,该NaOH溶液的浓度至少为0.96mol/L | |
| D. | 溶解4.08 g镁铝合金时,剩余盐酸的物质的量为0.1 mol |
1.已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中A、B同主族,B、C、D、E同周期,B的核外电子数为C的$\frac{1}{2}$,D的最外层电子数为C、E之和的一半.下列说法正确的是( )
| A. | A、B能形成离子化合物,且A离子半径小于B离子半径 | |
| B. | A、D能形成离子化合物DA5,与H2O反应能生成A的单质 | |
| C. | C、D的简单氢化物中只有D溶于水,其水溶液呈酸性 | |
| D. | E的两种氢化物中所有化学键种类完全相同 |
2.环丙叉环丙烷(A)结构特殊,根据如下转化判断下列说法正确的是( )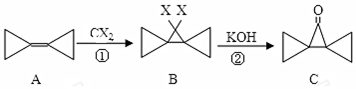
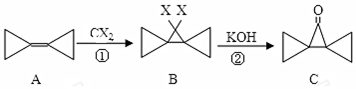
| A. | 反应①是加成反应 | B. | A的所有原子都在一个平面内 | ||
| C. | 反应②是消去反应 | D. | A的二氯代物只有2种 |

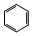 +3H2$\stackrel{催化剂}{→}$
+3H2$\stackrel{催化剂}{→}$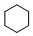
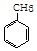 +3HO-NO2$→_{△}^{浓硫酸}$
+3HO-NO2$→_{△}^{浓硫酸}$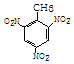 +3H2O,反应类型取代反应
+3H2O,反应类型取代反应 .
. .
.