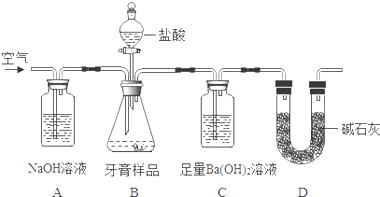
��Ŀ����
��ѧ�ҷ���ijҩ��M��������Ѫ�ܼ�������Ϊ�������������ͷų�һ�֡���ʹ���ӡ�D����������D�������ڵ�����ԭ����Ϊ�������ٻ���1998��ŵ��������ѧ��ҽѧ������ش��������⣺
��1����֪M����Է�������Ϊ227����C��H��O��N����Ԫ����ɣ�C��H��N��������������Ϊ15.86%��2.20%��18.50%����M�ķ���ʽ�� ��D��˫ԭ�ӷ��ӣ�������Ϊ30����D�ķ���ʽΪ ��
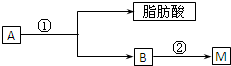
��2����֬A������;���ɵõ�M��
ͼ�Тڵ���ʾ��C2H5OH+HO-NO2
C2H5O-NO2+H2O
���� ��������
��Ӧ�ٵĻ�ѧ��Ӧ������ ����Ӧ�ڵĻ�ѧ����ʽ�� ��
��3��C��B��������һ�������·�Ӧ���ɵĻ����������Ϊ134��д��C���п��ܵĽṹ��ʽ ��
��4������0.1mol B�������Ľ����Ʒ�Ӧ���������� g�����ƣ�
��1����֪M����Է�������Ϊ227����C��H��O��N����Ԫ����ɣ�C��H��N��������������Ϊ15.86%��2.20%��18.50%����M�ķ���ʽ��
��2����֬A������;���ɵõ�M��

ͼ�Тڵ���ʾ��C2H5OH+HO-NO2
| Ũ���� |
���� ��������
��Ӧ�ٵĻ�ѧ��Ӧ������
��3��C��B��������һ�������·�Ӧ���ɵĻ����������Ϊ134��д��C���п��ܵĽṹ��ʽ
��4������0.1mol B�������Ľ����Ʒ�Ӧ����������
���㣺�л���Ľṹ������,�л���ʵ��ʽ�ͷ���ʽ��ȷ��,�л�����ƶ�
ר�⣺�л���Ļ�ѧ���ʼ��ƶ�
��������1����ԭ�ӵ����ʵ���֮�ȵ���ԭ�Ӹ���֮�ȣ����ݷ�����ԭ����ռ������������ȷ���л���ķ���ʽ��������Է���������ȷ�����ʵķ���ʽ��
��2����֬ˮ��IJ����Ǹ�֬������ͣ���Ӧ�ٵĻ�ѧ��Ӧ����Ϊˮ�⣻���������ʾ����Ӧ��Ϊ���͵�������Ӧ��
��3��C����B���������������ᷴӦ���ɵIJ����C��Է�������Ϊ134����B����Է�������Ϊ92��������Է�������Ϊ60���Ƶò���C����B�����ᰴ1��1��Ӧ���ã����ͣ������������������ǻ�������γɵ��������ֿ��ܵĽṹ��
��4�����ݸ������Ʒ�Ӧ����ʽ���������Ľ����Ƶ�������
��2����֬ˮ��IJ����Ǹ�֬������ͣ���Ӧ�ٵĻ�ѧ��Ӧ����Ϊˮ�⣻���������ʾ����Ӧ��Ϊ���͵�������Ӧ��
��3��C����B���������������ᷴӦ���ɵIJ����C��Է�������Ϊ134����B����Է�������Ϊ92��������Է�������Ϊ60���Ƶò���C����B�����ᰴ1��1��Ӧ���ã����ͣ������������������ǻ�������γɵ��������ֿ��ܵĽṹ��
��4�����ݸ������Ʒ�Ӧ����ʽ���������Ľ����Ƶ�������
���
�⣺��1��M����Է�������Ϊ227��C��H��N��������������Ϊ15.86%��2.20%��18.50%����
Cԭ�Ӹ���Ϊ��
��3��Hԭ�Ӹ���Ϊ��
��5��Nԭ�Ӹ���Ϊ��
��3��Oԭ�Ӹ���Ϊ��
=9�����Է���ʽΪC3H5O9N3��
D��˫ԭ�ӷ��ӣ���Է�������Ϊ30��ƽ��һ��ԭ�ӵ�ԭ����Ϊ15������DΪNO��
�ʴ�Ϊ��C3H5O9N3��NO��
��2����֬���Ǹ�֬���������������ˮ��õ���֬������ͣ�ˮ�ⷴӦ����ȡ����Ӧ����ӦΪ�� �����ͺ�HNO3���ո�������ʾ����������Ӧ���йط�Ӧ�Ļ�ѧ����ʽΪ��
�����ͺ�HNO3���ո�������ʾ����������Ӧ���йط�Ӧ�Ļ�ѧ����ʽΪ��
 ��
��
�ʴ�Ϊ��ȡ����Ӧ�� ��
��
��3��C����B���������������ᷴӦ���ɵIJ����C��Է�������Ϊ134����B����Է�������Ϊ92��������Է�������Ϊ60���Ƶò���C����B�����ᰴ1��1��Ӧ���ã����ͣ������������������ǻ�������γɵ��������ֿ��ܵĽṹ�� ��
��
�ʴ�Ϊ�� ��
��
��4�������������Ľ����Ʒ�Ӧ��2HOCH2CHOHCH2OH+6Na��2NaOCH2CHONaCH2ONa+3H2����0.1mol������0.3mol�ƣ�����Ϊm=n��M=0.3mol��23g/mol=6.9g��
�ʴ�Ϊ��6.9��
Cԭ�Ӹ���Ϊ��
| 227��15.86% |
| 12 |
| 227��2.20% |
| 1 |
| 227��18.50% |
| 14 |
| 227��(1-15.86%-2.20%-18.50%) |
| 16 |
D��˫ԭ�ӷ��ӣ���Է�������Ϊ30��ƽ��һ��ԭ�ӵ�ԭ����Ϊ15������DΪNO��
�ʴ�Ϊ��C3H5O9N3��NO��
��2����֬���Ǹ�֬���������������ˮ��õ���֬������ͣ�ˮ�ⷴӦ����ȡ����Ӧ����ӦΪ��
 �����ͺ�HNO3���ո�������ʾ����������Ӧ���йط�Ӧ�Ļ�ѧ����ʽΪ��
�����ͺ�HNO3���ո�������ʾ����������Ӧ���йط�Ӧ�Ļ�ѧ����ʽΪ�� ��
���ʴ�Ϊ��ȡ����Ӧ��
 ��
����3��C����B���������������ᷴӦ���ɵIJ����C��Է�������Ϊ134����B����Է�������Ϊ92��������Է�������Ϊ60���Ƶò���C����B�����ᰴ1��1��Ӧ���ã����ͣ������������������ǻ�������γɵ��������ֿ��ܵĽṹ��
 ��
���ʴ�Ϊ��
 ��
����4�������������Ľ����Ʒ�Ӧ��2HOCH2CHOHCH2OH+6Na��2NaOCH2CHONaCH2ONa+3H2����0.1mol������0.3mol�ƣ�����Ϊm=n��M=0.3mol��23g/mol=6.9g��
�ʴ�Ϊ��6.9��
���������⿼���л����ƶϣ��漰��֬�����ʡ�����������Ӧ��ͬ���칹����д�ȣ��Ѷ��еȣ�ע������ŵ����ʼ���ת����

��ϰ��ϵ�д�
�����Ŀ
���н�����ʵ��ʵ����������ӷ���ʽ����ȷ���ǣ�������
| A����ʳ�׳�ȥůˮƿ�е�ˮ����ˮ���ܽ⣬����ɫ���ݲ�����2CH3COOH+CaCO3�TCa2++2CH3COO-+CO2��+H2O |
| B����ϡ�����ȥͭ�̣�4H++Cu2��OH��2CO3=2Cu2++CO2��+3H2O |
| C����NaHCO3��CaCl2�����Һ�У���������NaOH��Һ��OH-+HCO32-�TCO32-+H2O |
| D����С�մ�����θ����ࣺHCO3-+H+�TH2O+CO2�� |
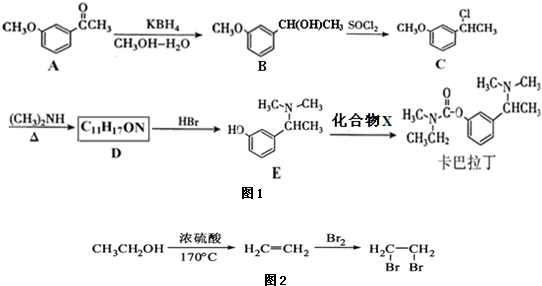
 ���ͱ�ͪ��
���ͱ�ͪ�� ���Ʊ�������
���Ʊ������� �ĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼ��ͼ2��
�ĺϳ�·������ͼ�����Լ���ѡ�����ϳ�·������ͼ��ͼ2��
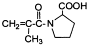 �ж���ͬ���칹�壬��
�ж���ͬ���칹�壬��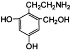 �ȣ�д��������������������ͬ���칹�壺A�����б�������������B������NaOH��Һ�����ʵ���֮��1��1��ȫ�кͣ�C��������һ±����ֻ��һ�֣�
�ȣ�д��������������������ͬ���칹�壺A�����б�������������B������NaOH��Һ�����ʵ���֮��1��1��ȫ�кͣ�C��������һ±����ֻ��һ�֣�